研究歷史
染料敏化太陽能電池的研究歷史可以追溯到19世紀早期的照相術。1837年,Daguerre制出了世界上第一張照片。兩年後,Fox Talbot將鹵化銀用於照片製作,但是由於鹵化銀的禁頻寬度較大,無法回響長波可見光,所以相片質量並沒有得到很大的提高。1883年,德國光電化學專家Vogel發現有機染料能使鹵化銀乳狀液對更長的波長敏感,這是對染料敏化效應的最早報導。使用有機染料分子可以擴展鹵化銀照相軟片對可見光的回響範圍到紅光甚至紅外波段,這使得“全色”寬譜黑白膠片乃至現在的彩色膠片成為可能。1887年,Moser將這種染料敏化效套用到鹵化銀電極上,從而將染料敏化的概念從照相術領域延伸到光電化學領域。1964年,Namba和Hishiki發現同一種染料對照相術和光電化學都很有效。這是染料敏化領域的重要事件,只是當時不能確定其機理,即不確定敏化到底是通過電子的轉移還是通過能量的轉移來實現的。直到20世紀60年代,德國的Tributsch發現了染料吸附在半導體上並在一定條件下產生電流的機理,才使人們認識到光照下電子從染料的基態躍遷到激發態後繼而注入半導體的導帶的光電子轉移是造成上述現象的根本原因。這為光電化學電池的研究奠定了基礎。但是由於當時的光電化學電池採用的是緻密半導體膜,染料只能在膜的表面單層吸附,而單層染料只能吸收很少的太陽光,多層染料又阻礙了電子的傳輸,因此光電轉換效率很低,達不到套用水平。後來人們製備了分散的顆粒或表面積很大的電極來增加染料的吸附量,但一直沒有取得非常理想的效果。1988年,Grätzel小組用基於Ru的染料敏化粗糙因子為200的多晶二氧化鈦薄膜,用Br2/Br-氧化還原電對製備了太陽能電池,在單色光下取得了12 %的轉化效率,這在當時是最好的結果了。直到1991年,Grätzel在O’Regan的啟發下,套用了O’Regan製備的比表面積很大的納米TiO2顆粒,使電池的效率一舉達到7.1 %,取得了染料敏化太陽能電池領域的重大突破。應當說,納米技術促進了染料敏化太陽能電池的發展。
結構組成
結構組成
主要由納米多孔半導體薄膜、染料敏化劑、氧化還原電解質、對電極和導電基底等幾部分組成。納米多孔半導體薄膜通常為金屬氧化物(TiO2、SnO2、ZnO等),聚集在有透明導電膜的玻璃板上作為DSC的負極。對電極作為還原催化劑,通常在帶有透明導電膜的玻璃上鍍上鉑。敏化染料吸附在納米多孔二氧化鈦膜面上。正負極間填充的是含有氧化還原電對的電解質,最常用的是I3/I-。
工作原理
染料敏化太陽電池結構示意圖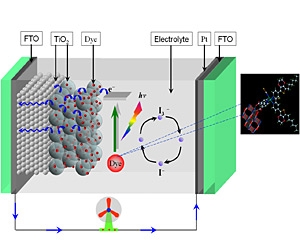 DSSC工作原理
DSSC工作原理 ⑴ 染料分子受太陽光照射後由基態躍遷至激發態;
⑵ 處於激發態的染料分子將電子注入到半導體的導帶中;
⑶ 電子擴散至導電基底,後流入外電路中;
⑷ 處於氧化態的染料被還原態的電解質還原再生;
⑸ 氧化態的電解質在對電極接受電子後被還原,從而完成一個循環;
⑹ 和 ⑺ 分別為注入到TiO2 導帶中的電子和氧化態染料間的複合及導帶上的電子和氧化態的電解質間的複合
研究結果表明:只有非常靠近TiO2表面的敏化劑分子才能順利把電子注入到TiO2導帶中去,多層敏化劑的吸附反而會阻礙電子運輸;染料色激發態壽命很短,必須與電極緊密結合,最好能化學吸附到電極上;染料分子的光譜回響範圍和量子產率是影響DSC的光子俘獲量的關鍵因素。到目前為止,電子在染料敏化二氧化鈦納米晶電極中的傳輸機理還不十分清楚,有待於進一步研究。
套用展望
通過近二十年的研究與最佳化,染料敏化太陽能電池的效率已經超過了13%。這種電池的突出優點是高效率、低成本、製備簡單,因此有望成為傳統矽基太陽能電池的有力競爭者。
 DSSC工作原理
DSSC工作原理
