基本介紹
- 中文名:抗衰蛋白FN
- 外文名:fibronectin
- 也稱:纖維連線蛋白
- 類型:一種大分子糖蛋白
FN簡介,作用原理,獲得獎項,
FN簡介
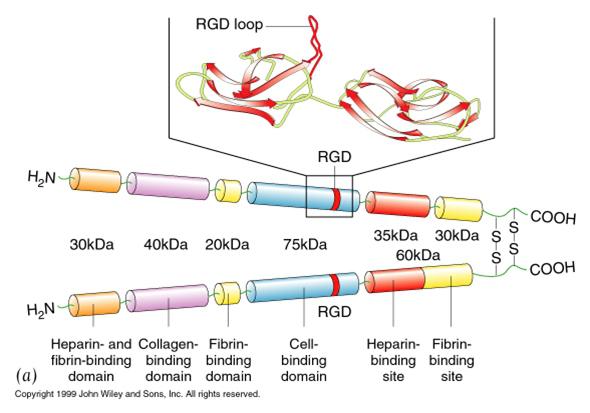
纖連蛋白,也稱纖維連線蛋白,英文名稱fibronectin(縮寫FN),是1974年國外研究發現的一種高分子糖蛋白,具有多種生物學功能。FN廣泛存在於動物組織和組織液中,是一種大分子糖蛋白,分子量約為450KD,具有多種生物活性。大量國內外的研究結果證明,FN分子在進化過程中保守性很強,各種動物體液中的FN具有非常相近的結構、性質和生物學功能,因而不同來源的FN可以相互替代使用。
纖連蛋白是一種細胞外基質中的高分子量糖蛋白,主要以三種形式存在,即由肝細胞或內皮細胞生成的血漿FN,由成纖維細胞、早期間充質細胞分泌合成的細胞FN,以及胎盤、羊膜組織中的胎兒FN。FN由兩個亞基通過C端的二硫鍵交聯形成,每個亞基的分子量為220~250kDa。
作為細胞外基質中重要的黏附分子之一,纖連蛋白與細胞膜上的整合素受體結合,在調節細胞黏附、遷移、增殖等過程中發揮著重要作用。纖連蛋白的異常表達與傷口癒合、腫瘤轉移、組織器官纖維化等密切相關。纖連蛋白的表達受到複雜的細胞信號通路網路控制,其中包括MAPK、PKC、JAK/STAT及JNK等。
作用原理
研究認為,細胞內外微循環障礙、細胞凋亡、免疫系統紊亂、自由基損傷等都會造成細胞衰老,進而影響機體衰老。FN從衰老根源細胞出發,有效緩解細胞衰老。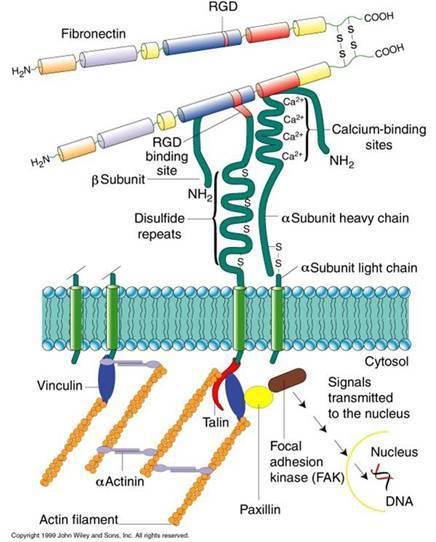 FN修復細胞作用圖
FN修復細胞作用圖
 FN修復細胞作用圖
FN修復細胞作用圖細胞內外微循環可供給細胞氧氣、營養物質及清除廢物,微循環障礙作為衰老象徵的結果與標誌,同時在促進器官、組織和整體衰老中起主要作用。纖連蛋白(fibronectin,FN)能夠全面修復各類細胞,激發細胞活力,提升細胞自體代謝功能,調節細胞與細胞間質之間的動態平衡,改善細胞內外微循環。纖連蛋白通過與細胞膜上的整合素受體結合,可以調節細胞的黏附、遷移、增殖,加速新陳代謝,促進細胞更新。
細胞凋亡是機體調控自身細胞增殖和死亡之間平衡的過程,細胞凋亡與衰老密切相關。當細胞喪失新陳代謝能力而不能及時被清除機體時,就會“堵塞”正常細胞的代謝空間,進而干擾新生細胞的產生,最終導致機體衰老。纖連蛋白(FN)通過調節細胞凋亡對衰老起到阻礙作用:一、FN廣泛參與細胞的遷移、黏附和增殖過程,促進細胞分裂增殖,更新細胞數量;二、FN調動單核吞噬細胞系統清除死亡細胞及細胞代謝廢物,為新生細胞的新陳代謝提供良好的內外環境。
免疫系統紊亂是機體衰老的重要原因。免疫學說認為在衰老過程中,機體的免疫功能明顯降低。纖連蛋白(FN)利用其遷移細胞的功能,調動T淋巴細胞與B淋巴細胞有序分布,刺激淋巴細胞產生免疫抗體,從而改善機體的免疫系統,阻礙機體衰老。0
機體有氧代謝過程中不斷產生超氧自由基(活性氧),它有很強的氧化作用,會破壞生物膜(質膜、細胞膜)與蛋白質結構,擾亂內分泌與免疫系統,加速機體衰老進程。纖連蛋白(FN)具有刺激細胞合成、分泌超氧化物歧化酶(SOD)、過氧化氫酶的功能,在抗氧化酶的活性與濃度降低時,它能夠利用其信號傳導機制向細胞發出合成超氧化物歧化酶(SOD)與過氧化氫酶的信息,再通過細胞膜的“外排”特性,將超氧化物歧化酶(SOD)與過氧化氫酶釋放到細胞外,清除機體內過多的超氧自由基,抑制氧化作用,保護生物膜(質膜、細胞膜)與蛋白質結構,延緩機體衰老。
獲得獎項
2012年,英國科學家約翰·戈登與日本科學家山中伸彌共同獲得諾貝爾生理學或醫學獎。他們在“體細胞重編程技術”領域做出了革命性貢獻,徹底改變了人們對細胞和器官生長的理解。他們認為,一些引導細胞運行的蛋白質(比如纖連蛋白,fibronectin,FN)能夠有助於成熟體細胞的重編程,因為重編程過程需要良好的細胞信號傳導機制。
2013年10月7日,諾貝爾獎官方網站報導,2013諾貝爾生理學或醫學獎今日公布,得主為美國科學家詹姆斯·羅斯曼、蘭迪·謝克曼和德國科學家托馬斯·聚德霍夫因,得獎原因是他們解開了細胞內的運輸機制之謎。
生物體內每一個細胞都是一個生產和輸出分子的工廠。比如,胰島素在這裡被製造出來並釋放進入血液當中,神經傳遞素從一個神經細胞傳導至另一個細胞。這些分子在細胞內都是以“小包”的形式傳遞的,這就是“細胞囊泡”。他們發現纖連蛋白(fibronectin,FN)可以讓囊泡實現與其目標細胞膜的對接和融合。在融合過程中,囊泡上的纖連蛋白和細胞膜上的纖連蛋白相互結合,就像分開的拉鏈相互咬合一樣,確保了各種物質只會被運輸到設定的位置上而不會出現錯誤。這一機制不管是在內部細胞器之間的運輸,還是向外的運輸過程中都會起作用。
除了發現地理位置上精準輸送的機制外,他們還發現時間上的精準輸送機制。從上世紀90年代起,托馬斯·聚德霍夫便開始在神經細胞中尋找對鈣離子敏感的蛋白質。最終他識別出一種分子機制,其會對注入的鈣離子做出反應,並控制鄰近的纖連蛋白(fibronectin,FN)迅速讓囊泡與神經細胞的外部細胞膜相結合。於是“拉鏈”打開了,信號物質被釋放出去。托馬斯·聚德霍夫的發現解釋了這種細胞傳輸的時間精確性是如何實現的,以及囊泡中的物質是如何實現受控地釋放。