選擇性
基因藥物具有很高的選擇性。一種基因藥物並不是適用於所有的人種,不同人種的基因存在較多差別。暫且不說白人、黑人、黃種人之間的基因差別,就連我國南方人和北方人都存在基因差異。例如鐮刀形
貧血病在黃種人中發現很少,但在白人和黑人中發病率很高,原因是白人和黑人體內有一種寄生蟲,治療鐮刀形
貧血症的藥物能使患者體內產生一種抗體,從而抵禦寄生蟲。因此,這種治療鐮刀形貧血症的基因藥物只能給白人和黑人服用。
另外,不同的生活環境也需要不同的基因藥物。如人們最渴望用基因治療的癌症,也有環境特性:
肝癌在亞洲發病率較高,肺癌、胃癌、
食管癌、肝癌是中國人多發的頑症,而直腸癌則是美國發病率最高的癌症。因此,環境也是研製基因藥物最重要的內容之一。
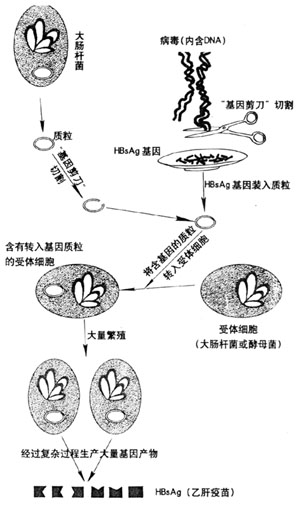 基因工程藥物模式圖
基因工程藥物模式圖如果我國製藥業仍然以仿製為生,那么到時候,基因藥物不但不能治病,反而要變成生命“殺手”了,後果將會不堪構想。我國製藥行業的首要任務是,如何提高自己的製藥技術,爭取生產出適合我國人們使用的基因藥物。
誕生
基因藥物的出現與基因工程技術的發展息息相關,基因工程技術是現代生物技術的主體。基因工程是通過對核酸分子的插入、拼接和重組而實現遺傳物質的重組,再藉助病毒、細菌、質粒或其他載體,將目的基因轉移到新的宿主細胞,並使目的基因在新的宿主細胞內複製和表達的技術。基因是DNA分子上的一個特定的片斷,因此基因工程又稱DNA分子水平上的生物工程。
現代遺傳學家認為,基因是DNA(脫氧核糖核酸)分子上具有遺傳效應的特定核苷酸序列的總稱,是具有遺傳效應的DNA分子片段。基因位於
染色體上,並在染色體上呈線性排列。基因不僅可以通過複製把遺傳信息傳遞給下一代,還可以使遺傳信息得到表達。不同人種之間頭髮、膚色、眼睛、鼻子等不同,是基因差異所致。
人類只有一個基因組,大約有5-10萬個基因。
人類基因組計畫是美國科學家於1985年率先提出的,旨在闡明人類基因組30億個鹼基對的序列,發現所有人類基因並搞清其在染色體上的位置,破譯人類全部遺傳信息,使人類第一次在分子水平上全面地認識自我。計畫於1990年正式啟動,這一價值30億美元的計畫的目標是,為30億個鹼基對構成的人類基因組精確測序,從而最終弄清楚每種基因製造的蛋白質及其作用。打個比方,這一過程就好像以步行的方式畫出從北京到海'>上海的路線圖,並標明沿途的每一座山峰與山谷。雖然很慢,但非常精確。
隨著人類基因組逐漸被破譯,一張生命之圖將被繪就,人們的生活也將發生巨大變化。基因藥物已經走進人們的生活,利用基因治療更多的疾病不再是一個奢望。因為隨著我們對人類本身的了解邁上新的台階,很多疾病的病因
將被揭開,藥物就會設計得更好些,治療方案就能“對因下藥”,生活起居、飲食習慣有可能根據基因情況進行調整,人類的整體健康狀況將會提高,二十一世紀的醫學基礎將由此奠定。
其主要任務是有關基因的分離、合成、切斷、重組、轉移和表達等。近20年來,DNA重組技術與基因治療技術發展十分迅速,已進入實用化階段。DNA重組技術的進展,大大增進了人們對生命本質的認識,包括對
疾病遺傳基礎的了解。今後對癌症的發生機制,疾病的遺傳特性,免疫系統的功能,代謝衰竭性疾病的病因和大腦功能的物化機理獲得進一步的了解,從而誕生對
遺傳性疾病和重大疑難疾病治療的新途徑。基因藥物就是基因工程技術發展的產物。它的出現將使現有的醫療實踐發生革命性的改變,使一切疾病變得可為人們征服。人們渴望的遠離疾病,而擁有健康體魄的時代正向我們走來。
發展
基因藥物隨著基因工程技術的發展而發展,大致經歷了3個階段:
細菌基因工程
它是通過原核細胞(常用大腸桿菌)來表達目的基因的,這個工程相當複雜,成本和工藝上也有許多問題。
細胞基因工程
細胞基因工程也有不足之處,因為人或哺乳動物細胞培養的條件相當苛刻,成本太高,這樣就限制了細胞基因工程的發展。
轉基因動物
即把人或哺乳動物的某種基因導入到哺乳動物的受精卵里,每個細胞里都帶有導入的基因,而且能穩定地遺傳到下一代。這樣一種新的個體,稱為轉基因動物。轉基因動物的問世,為利用新的基因工程手段獲得低成本高活性的基因藥物開闢了一條新的途徑。
合成生物學
通過計算機輔助設計最佳化次生代謝反應鏈,人工合成基因調控網路,從而實現工程菌或酵母細胞內表達外源藥用生物分子的代謝工程,尤其是
天然藥物次生代謝藥物分子,比如,2003年美國貝克利大學成功在酵母細胞內表達植物藥物分子青篙素等。
動物藥廠
概念
科學家發現,人類的很多先天性疾病是由於缺乏與之相應的基因造成的,而靠一般的藥物很難治癒,如將正常人的正常基因片段導入到動物體內,讓這種基因在哺乳動物體內表達,就可從該動物分泌的乳汁或者其他組織提取獲得具有活性的基因藥物,用於治療該基因缺損造成的疾病。這種通過轉基因動物獲取藥物的方法稱為動物藥廠。
動物藥廠改變了人們對藥廠的印象。它看起來更像是一個牧場。在這裡,成群的轉基因牛羊在綠色的草地上吃草,表面看,它們與普通牛羊沒有差異,然而,它們體內分泌的乳汁是能給人類治病的藥品,這些產乳量高的動物,就相當於一座大型的藥物工廠,以它們廉價的乳汁,為人類提供著大量的所需要的珍貴藥物。
經濟意義
據專家預測,下世紀疾病的基因治療將大規模地從試驗進入臨床套用。屆時,利用生物技術生產的藥物將大量問世,生物製藥業將成為21世紀發展最快的高科技產業之一。生物高技術醫藥工業雖具有強投資、長周期、高風險的特點,但一經產業化就會帶來高額利潤,與傳統醫藥產業相比、動物藥廠更具有投資少、效益高、無公害等優點。
醫學遺傳家曾益滔介紹,做細菌基因工程需要很大的車間發酵;做細胞工程藥物也需要很多昂貴的設備來培養細胞,而若用轉基因動物,就只要飼養,動物乳汁便可源源不斷地產出藥品。
研製一種新藥,一般需要20年——30年,即使科技再發展,也很難低於10年——15年,轉基因羊周期一般是18周,牛也只需2年——3年,而效益更是驚人。如荷蘭金髮馬公司用轉基因牛生產的一種乳鐵蛋白,製成奶粉具有轉鐵、抗菌等功能,預計每年這一營養奶粉銷售額是50億美元。
1998年2月上海醫學遺傳研究所試驗成功的轉基因山羊所表達的“
凝血因子”如進入工業生產也將具有驚人的產值。據美國資料統計,過去凝血因子Ⅶ都是從獻血的血源中提取的,全美國這方面的病人一年需求約為120g左右,這120g得從120萬升的血漿中提取,以每人獻血200ml計,就需要600萬個獻血者提供血漿。若改用轉基因牛來生產,只需1.2頭牛產的牛乳即可滿足。
轉基因動物帶來的這場生物醫藥革命,不僅產生了巨大的經濟效益,而且還使人們傳統的醫療方式發生變化,人們可以一邊喝著鮮美的牛奶,一邊達到了治病的目的,這個質的變化不能不令人心動。
成就
基因重組技術取得了一個個豐碩成果。1978年合成了人工胰島素,1979年實現了
生長激素基因在大腸桿菌中的表達,1982年研製成功了人工
干擾素,基因製藥從此走上了產業化道路。但是,基因藥物是通過基因重組技術培育大腸桿菌和動物細胞來製造的,而大腸桿菌這類低等生物是不可能生產出結構複雜的藥物,動物細胞培養的成本又太高。所以,利用基因重組與移植技術來培育轉基因動物生產藥物便應運而生了在利用轉基因動物提取藥物方面,英國科學家首開先河。1997年年底,英國PPL治療學公司率先利用克隆"多利"所採用的"細胞核轉變"法,培育出200頭攜帶人體基因的綿羊,並成功地從奶汁中提取了α-1抗胰蛋白酶。這是科學家首次從遺傳工程培育的綿羊的奶中,提取可用於治療人類疾病的藥物成分,為建立"動物藥廠" 打下了基礎。隨後,芬蘭科學家將人體的促紅細胞生長素基因,植入乳牛的受精卵中,創造了一種能生產出促紅細胞生長素的乳牛。從理論上說,這種乳牛一年可提取60-80千克促紅生長素,比全世界的使用量還多。
風險
基因組藥物的運用,將在醫學上產生革命性的變化。藥物將針對具體的每一個人,治療效率變得更高,並且更省錢。”科學家這樣告訴我們理解DNA。但我們距離那一天還很遙遠。
《科學》雜誌最近報導,科學家們樂觀估計,要到2053年(DNA雙螺旋結構發現100周年時),或者最樂觀的估計是在2020年,才可能有基因組藥物出現。
科學家一致認為,我們還沒到達利用基因信息直接生產回響藥物的地步。換言之,我們還沒有跨入真正的基因時代。測試完成僅僅是開始“我們經常會碰到人們提問,當人類基因組序列測試完成的時候會怎樣?以前通常的回答是:這將極大地促進藥物的開發;預防性藥物的時代即將來臨;針對個人的療法將得到推廣;人類壽命將拉長。而我們已經知道,人類基因組序列測試的完成,其實僅僅是一個開始。”美國科學家新德里·波瑞納說。
這種觀點得到了中國科學家的認同。華大基因研究中心副主任、研究員談學海說:“基因組藥物的普遍套用當然是更為遙遠的事。對人類整個基因組的認識、分析基因和各種疾病之間的關係都是巨大的工程,而讓整個醫學界跟上‘基因醫學’的步伐更不是一朝一夕能夠辦到的事。”
“當人類和一些病原體基因工程部分完成的時候,有人認為在20年後,人類醫藥將發生翻天覆地的變化;一些頑強的人類健康殺手將得到有效的控制。但當我們慶祝DNA雙螺旋分子結構發現50周年的時候,我們清楚地認識到,這樣的認識很不成熟。”牛津大學分子藥學學院的戴維德教授說。
如果我們人體生理學方面的知識沒有取得決定性的進展,那DNA序列的測試將變得毫無意義。“我們必須了解,生病的時候,人體內部發生了怎樣的變化,我們要怎樣去干預、治療以及預防。對於未來的藥物,我們需要紮實的知識和信息來分析基因和各種疾病之間的關係,至少對於一些常見病需要能夠弄清楚這些關係;此外,我們還需了解一些外在因素對疾病的影響。”
科學家認為,在未來,更多情況下障礙還是來自生物的多樣性,即不同的人種帶來的差異問題。
大概在30年前,醫生開始使用一種強力殺死細胞的藥物來治療患白血病的兒童。這種叫做6-巰基嘌呤(6MP)的藥物拯救了成千上萬的生命。然而,這種藥物會產生一定的副作用。早在20多年前就已經研究發現,它的毒素能夠滯留病人體內,並且會遺傳。這種藥物能夠迅速積累,然後滲入骨髓,進而產生感染。
不同的人種,這種酶缺陷的人所占比例是不一樣的。例如,在高加索人中,每300個人中就有一個這樣的人,這樣的人是不能接受6MP治療的,否則會帶來致命的危險。
這種困惑將是未來的基因組藥物普遍遇到的問題,基因藥物的風險是肯定的。
相關製劑
由於基因藥物的高效性,可以用它將人們改造得身強體健,所以有些為了創造成績不顧一切的運動員和教練就開始鋌而走險,打起了基因藥物的主意。利用
基因技術改造人體風險很大,所以體育協會將基因興奮劑列入禁止名單,嚴格禁止使用。
 基因工程藥物模式圖
基因工程藥物模式圖
 基因工程藥物模式圖
基因工程藥物模式圖