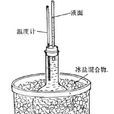
反常膨脹,是指一般物質由於溫度影響,其體積為熱縮冷脹。
如水,銻, 熔融的二氧化矽, 立方氧化鋯鎢
水的反常膨脹現象可以用氫鍵、締合水分子理論予以解釋。 只有在0℃到4℃的範圍內的水才顯示出反常膨脹的現象來。
基本介紹
- 中文名:反常膨脹
- 外文名:Anomalous expansion
- 拼音:fan chang peng zhang
- 相對概念:熱脹冷縮
- 作用量:溫度
- 相關物質:水、銻、鉍、液態鐵等
現象說明,名詞解釋,締合水分子,呈現方法,熱脹冷縮,水的反常膨脹,
現象說明
0℃~4℃ 熱縮冷脹
4℃以上 熱脹冷縮
(4℃時體積最小,密度最大)
詳義:
一般物質由於溫度影響,其體積為熱脹冷縮。但也有少數熱縮冷脹的物質,如水、銻、鉍、液態鐵等,在某種條件下恰好與上面的情況相反。實驗證明,對0℃的水加熱到4℃時,其體積不但不增大,反而縮小。當水的溫度高於4℃時,它的體積才會隨著溫度的升高而膨脹。因此,水在4℃時的密度最大。湖泊里水的表面,當冬季氣溫下降時,若水溫在4℃以上時,上層的水冷卻,體積縮小,密度變大,於是下沉到底部,而下層的暖水就升到上層來。這樣,上層的冷水跟下層的暖水不斷地交換位置,整個的水溫逐漸降低。這種熱的對流現象只能進行到所有水的溫度都達到4℃時為止。當水溫降到4℃以下時,上層的水反而膨脹,密度減小,於是冷水層停留在上面繼續冷卻,一直到溫度下降到0℃時,上面的冷水層結成了冰為止。以上階段熱的交換主要形式是對流。當冰封水面之後,水的冷卻就完全依靠水的對流方式來進行熱傳遞。由於水的導熱性能很差,因此湖底的水溫仍保持在4℃左右。這種水的反常膨脹特性,保證了水中的動植物,能在寒冷季節內生存下來。這裡還應注意到,冰在冷卻時與一般物質相同,也是縮小的。受熱則膨脹,只有在0℃到4℃的範圍內的水才顯示出反常膨脹的現象來。
名詞解釋
水的反常膨脹現象可以用氫鍵、締合水分子理論予以解釋。
物質的密度由物質內分子的平均間距決定。對於水來說,由於水中存在大量單個水分子,也存在多個水分子組合在一起的締合水分子,而水分子締合後形成的締合水分子的分子平均間距變大,所以水的密度由水中締合水分子的數量、締合的單個水分子個數決定。具體地說,水的密度由水分子的締合作用、水分子的熱運動兩個因素決定。當溫度升高時,水分子的熱運動加快、締合作用減弱;當溫度降低時,水分子的熱運動減慢、締合作用加強。綜合考慮兩個因素的影響,便可得知水的密度變化規律。
締合水分子
在水中,常溫下有大約50%的單個水分子組合為締合水分子,其中雙分子締合水分子最穩定。
多個水分子組合時,除了呈六角形外(如雪花、窗花),還可能形成立體形點陣結構(屬六方晶系)。每一個水分子都通過氫鍵,與周圍四個水分子組合在一起。圖中只畫出了中央一個水分子同周圍水分子的組合情況。邊緣的四個水分子也按照同樣的規律再與其他的水分子組合,形成一個多分子的締合水分子。締合水分子中,每一個氧原子周圍都有——4個氫原子,其中兩個氫原子較近一些,與氧原子之間是共價鍵,組成水分子;另外兩個氫原子屬於其他水分子,靠氫鍵與這個水分子組合在一起。可以看出,這種多個分子組合成的締合水分子中的水分子排列得比較鬆散,分子的間距比較大。由於氫鍵具有一定的方向性,因此在單個水分子組合為締合水分子後,水的結構發生了變化。一是締合水分子中的各單個分子排列有序,二是各分子間的距離變大。
呈現方法
在液態水變成固態水時,即水凝固成冰、雪、霜時,呈現出締合水分子的形狀。此時,水分子的排列比較“鬆散”,雪、凍的密度比較小。
將冰熔化成水,締合水分子中的一些氫鍵斷裂,凍的晶體消失。0℃的水與0℃的冰相比,締合水分子中的單個水分子數目減少,分子的間距變小、空隙減少,所以0℃的水比0℃的冰密度大。用倫琴射線照射0℃的水,發現只有15%的氫鍵斷裂,水中仍然存在有約85%的微小冰晶體(即大的締合水分子)。若繼續加熱0℃的水,隨著水溫度的升高,大的締合水分子逐漸瓦解,變為三分子締合水分子、雙分子締合水分子或單個水分子。這些小的締合水分子或單個水分子,受氫鏈的影響較小,可以任意排列和運動,不必形成“鏤空”結構,而且單個水分子還可以“嵌入”大的締合水分子中間。在水溫升高的過程中,一方面,締合數小的締合水分子、單個水分子在水中的比例逐漸加大,水分子的堆集程度(或密集程度)逐漸加大,水的密度也隨之加大。另一方面在這個過程中,隨著溫度的升高,水分子的運動速度加快,使得分子的平均距離加大,密度減小。考慮水密度隨溫度變化的規律時,應當綜合考慮兩種因素的影響。在水溫由0℃升至4℃的過程中,由締合水分子氫鍵斷裂引起水密度增大的作用,比由分子熱運動速度加快引起水密度減小的作用更大,所以在這個過程中,水的密度隨溫度的增高而加大,為反常膨脹。
熱脹冷縮
水溫超過4℃時,同樣應當考慮締合水分子中的氫鍵斷裂、水分子運動速度加快這兩個因素,綜合分析它們對水密度的影響。由於在水溫比較高的時候,水中締合數大的締合水分子數目比較小,氫鍵斷裂所造成水密度增加的影響較小,水密度的變化主要受分子熱運動速度加快的影響,所以在水溫由4℃繼續升高的過程中,水的密度隨溫度升高而減小,即呈現熱脹冷縮現象。
在4℃時,水中雙分子締合水分子的比例最大,水分子的間距最小,水的密度最大。
水的反常膨脹
液態水,除含有簡單的水分子(H2O)外,同時還含有締合分子(H2O)2和(H2O)3等,當溫度在0℃水未結冰時,大多數水分子是以(H2O)3的締合分子存在,當溫度升高到3.98 ℃(101 kPa)時,水分子多以(H2O)2締合分子形式存在,分子占據空間相對減小,此時水的密度最大。如果溫度再繼續升高在3.98 ℃以上,一般物質熱脹冷縮的規律即占主導地位了。水溫降到0 ℃時,水結成冰,水結冰時幾乎全部分子締合在一起成為一個巨大的締合分子,在冰中水分子的排布是每一個氧原子有四個氫原子為近鄰(兩個共價鍵,兩個氫鍵)。這樣一種排布導致成一種敞開結構,也就是說凍的結構中有較大的空隙,所以凍的密度反比同溫度的水小。