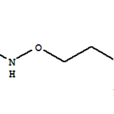
氨酸簡介
canavanine
在
精氨酸酶作用下可分解為副刀豆氨酸〔canaline,NH
2OCH
2CH
2CH(NH
2)COOH〕和尿素,另外在轉脒基酶的作用下則生成高絲氨酸〔CH
2(OH)CH
2CH(NH
2)COOH〕和羥基胍〔NH
2C(=NH)NHOH〕。
刀豆氨酸的結構與精氨酸相似,動物攝入會導致刀豆氨酸代替精氨酸合成蛋白質,由於刀豆氨酸與精氨酸結構的不同,所形成蛋白質的功能也會出現異常,最終導致動物死亡。
發現
刀豆氨酸最早是在1939年由日本科學家Kitagawa 和Tomiyamo 在研究哺乳動物肝中尿酸的形成過程中發現的並將其命名為canavanine。隨後Gulland和Morris以及Kitagawa[提出用化學方法製取刀豆氨酸,後來經完善,成功地利用化學方法製取出刀豆氨酸。到了六十年代初期刀豆氨酸的消旋性也被發現,即 L-刀豆氨酸(L-canavanine)和 D-刀豆氨酸(D-canavanine)。
製備
隨著刀豆氨酸消旋性的發現,Damadara 等於1939 年成功地從脫油脂的豆科植物種子中提取出刀豆氨酸。直到1971 年Hunt 和Thompson通過離子交換色譜法提取出了純度高的、具有消旋性的 L-刀豆氨酸,由於這些提取方法有太多不足比如提取率低下或純度也不高。1977 年,Rosenthal 等利用植物提取法直接從刀豆中提取出了較高純度的 L-刀豆氨酸。後來,人們大都採用此方法提取刀豆氨酸,還有學者將此方法進行了改良;另外自刀豆氨酸發現以來就有不少研究者進行了化學合成研究,
現將利用化學合成方法提取刀豆氨酸的研究敘述如下:
(1)Rosenthal 等於1985年以 L-蛋氨酸為原料合成 L-副刀豆氨酸,後來又進一步合成刀豆氨酸,且於 1995年對其合成方法進行了改進完善。該方法以 L-蛋氨酸為原料,經過環化合成重要中間體 L-2-[(苄氧羰基)氨]-4-丁內酯,這一過程是以氯甲酸苄酯為保護氨基試劑,再經過開環、羥基保護、脫保護劑等過程合成 L-刀豆氨酸。這一方法優點是原料廉價且易得,其收率高為 67%,缺點是過程複雜,對儀器設備要求較高,反應條件難控制,對環境有污染。
(2)Frankal.M 等於1963 年運用 γ-丁內酯合成 DL-刀豆氨酸法:該方法只有一步反應生成中間體 DL-α-苯氨基-γ-丁內酯,這一方法優點是反應步驟比較簡單,缺點是反應收率低,只有 28.5%,而且最終產物只得到 DL-刀豆氨酸,還需進一步進行手性拆分,如果能找到合適的拆分劑也將是非常好的方法。
(3)由L-高絲氨酸製備 L-刀豆氨酸法。這一方法主要是以 L-高絲氨酸為原料,氨基保護試劑為碳酸二叔丁酯,合成過程與方法1 相類似,合成 L-刀豆氨酸。該方法的優點是合成中間體的產率較高,氨基保護劑毒性小,反應收率為 51%。缺點是 L-高絲氨酸價格昂貴,作為原料成本高,進一步工業化不適宜。
分布
刀豆氨酸並不是在數量和質量上、時間和空間上會均勻的分布於整個植株,在不同的生長發育時期,其分布也在發生變化,其濃度也在不斷的變化。1978年,Bell報導了L-刀豆氨酸普遍存在於豆科的240屬,1200種植物中。在一些豆科植物種子中L-刀豆氨酸含量極高[26~28]。In Doo Hwang等報導指出利用光電特異反應法分析了在完整的刀豆植物(C.lineata)中發現了刀豆氨酸,其葉片中刀豆氨酸含量為7.89μmol/ g FW,根中刀豆氨酸含量為4.50μmol/g FW。據報導刀豆氨酸在刀豆(C.ensiformis)種子中占乾重的4%,並且刀豆氨酸和可溶性氮的運輸和儲存是一致的。還有報導指出刀豆種子中刀豆氨酸含量占總乾重的10%和總氮含量的55%以上。
功能
刀豆氨酸對昆蟲的作用
一些昆蟲取食含有不同量的刀豆氨酸的食物,表現出不同的反應。據報導根據昆蟲對刀豆氨酸的反應程度可以將它們分為三種類型,分別是:能夠利用刀豆氨酸的昆蟲,如一種象鼻蟲(Caryedes brasiliensis),它不僅能降解刀豆氨酸的毒性,還能將刀豆氨酸轉化成氮源加以利用;抗刀豆氨酸的昆蟲,如美洲菸夜蛾(Helithis virescens),在一定的劑量範圍內,這類昆蟲具有降解刀豆氨酸毒性的能力;敏感性昆蟲,如菸草天娥(Manduca sexta),這類昆蟲研究的最多還包括有斜紋夜蛾(Spodoptera litura)。Koul研究發現L-刀豆氨酸不僅能直接殺死菜蛾幼蟲,還能減輕幼蟲的體重延緩幼蟲的生長發育以致造成蛹及成蟲的畸形試驗過程中他們發現,當以菸草天蛾(M.sexta)幼蟲為試蟲飼餵含有L-刀豆氨酸的人工飼料時,試蟲的發育速率有所降低,甚至部分幼蟲直接死亡,而且殘存幼蟲體重減輕,不能正常化蛹和羽化。所以L-刀豆氨酸對菜蛾幼蟲有一定的拒食作用甚至是毒殺作用。同時其對玉米螟(O strinia furnacalis)生殖力也有明顯的抑制作用。而且具有克服菜蛾對擬除蟲菊酯抗藥性的作用。特別是目前菜蛾對擬除蟲菊酯普遍產生抗藥性的情況下。
此外,刀豆氨酸還影響一些昆蟲的取食行為,比如對大菜青蟲(Pieris brassicae)表現有忌避和拒食作用。刀豆氨酸的作用與克百威相比其藥效是較低的、緩慢的,儘管刀豆氨酸的毒力相對較低,作用緩慢,用量較高,但也不能忽視L一刀豆氨酸作為殺蟲劑的潛在可能性,主要是由於其實驗所用的L-刀豆氨酸是從刀豆種子中直接提取出來的,沒有合適的劑型化或增效化。刀豆氨酸的某些特性阻礙了它的發展的步伐,主要表現在它的作用緩慢、用藥量較高等方面。然而在看到其缺點同時也要看到它的優點,其優點表現在毒性低,易降解為無污染的物質有利於保護自然,從它的作用機制出發判斷出它不損害害蟲的寄生性天敵,因而有利於保護害蟲天敵昆蟲。目前存在的問題是如何使其劑型化或者說增效化,也許可以利用遺傳工程,使植株自身產生刀豆氨酸來抵禦害蟲侵襲,這也許是抗害蟲的另外一個途徑。所以利用植物次生性代謝產物刀豆氨酸製成植物源殺蟲劑或許可以減少化學農藥對環境的污染和降低化學農藥投入量,在病蟲害防治方面體現出可持續發展,同時也有利於促進植物次生代謝物質類特別是植物保護劑的開發和利用。
刀豆氨酸的抗代謝作用及其機制
據報導在病毒、細菌、真菌以及較低和較高的植物和動物中都發現了L-刀豆氨酸具有較強的抗代謝性,其抗代謝性體現在L-刀豆氨酸是L-精氨酸的類似物,二者分子結構極其相似,所以它可替代精氨酸參與蛋白質的合成反應,因為在蛋白質合成的過程中精氨酸-t RNA合成酶錯誤地將刀豆氨酸當成是精氨酸進行識別,從而將刀豆氨酸合成到初期多肽鏈中,含有刀豆氨酸的多肽鏈進一步摺疊成蛋白質,且最終打亂了DNA和RNA的正常代謝過程,進而影響含精氨酸的蛋白質的正常代謝過程,合成具有生理功能不全的蛋白質,因而具有良好的抗腫瘤性,特別是對於胰腺癌具有較好的治療效果。胰腺癌是一種非常嚴重的消化道系統的惡性腫瘤,在美國,胰腺癌位於惡性腫瘤死亡原因的第4位,居於消化道腫瘤死亡原因的第2位。隨著癌症越來越危害著人類身體健康的時候,目前在植物次生代謝產物中尋找新的毒性低且療效高的抗癌活性成分,是尋找抗腫瘤藥物最為活躍的研究領域之一。所以在植物中探索抗癌新藥,具有廣闊的前景。因此,L-刀豆氨酸作為一種抗癌特別是抗胰腺癌物質具有廣闊的研究價值。
刀豆氨酸作為潛在殺蟲劑的優點
植物源農藥作為生物合理性農藥的一個重要組成部分,目前越來越受到人們的廣泛重視,研究開發和利用植物資源套用於害蟲防治方面具有廣闊的前景。植物源農藥由於其毒性低,殘留少,對環境無污染等優點而被廣泛地套用。它可替代一些化學合成的農藥來防治菜蛾等害蟲,但是L-刀豆氨酸的某些特性阻礙了這方面發展的步伐,主要表現在其作用緩慢,用藥量比較高,如郝赤(1996)在室內通過葉片飼餵法測得了L-刀豆氨酸對菜峨敏感與抗性品系4齡幼蟲的LC50劑量分別為2610.99mg/L和3026.77mg/L。L-刀豆氨酸表現出較緩慢的毒殺作用,可能與其作用機制有關,另一個原因可能是實驗用的L-刀豆氨酸只是從豆科種子中的直接提取出來的,並沒有合適的劑量化。另外,L-刀豆氨酸在創傷性休克中具有重要作用,可以減輕腸道內內毒素、細菌的移位,而且還能改善線粒體功能和有氧代謝活動,對休克的治療具有非常重要的意義[57]。因此,植物次生代謝產物在保護植物避免遭受昆蟲、病原菌的侵害中發揮了很重要作用。研究植物次生代謝產物的合成途徑、調控機制等以及闡明植物與其他生物間的關係,有利於保護農業、果蔬產品,同時對農業改進生態環境和農業可持續發展都具有重要的理論指導和實踐意義。
測定方法
Fearon等於1955年發現Pentacyanoammonioferrate(PCAF)能與刀豆氨酸發生特異性顯色反應,生成比較穩定的品紅色。後來這就成了鑑定刀豆氨酸特異反應的一種方法。根據已報導的測定刀豆氨酸的方法,主要是運用PCAF與L-刀豆氨酸的特異反應[59]的光電比色法和HPLC法以及胺基酸自動分析儀法對刀豆氨酸進行定量測定。但由於比色法靈敏度比較差,經過改進後用胍類化合物與菲醌形成螢光環體系,但是由於精氨酸的干擾,這一方法不適宜用於刀豆氨酸的定量分析。同時試劑PCAF Sigma公司早已停止生產,HPLC所採用的衍生劑有鄰苯二甲醛(OPA),丹醯氯(Dansyl - Cl)等,這些都是很複雜的測定刀豆氨酸的方法,對儀器要求也比較高,同時都存在不足之處。所以需要尋找一種新的、簡單快速測定的方法。
合成代謝途徑
1982年Rosenthal[64]利用同位素標記法發現在Jack Bean,Canavalia ensiformis(L.)植物中L-刀豆氨酸(L-canavanine)的合成是由L-副刀豆氨酸(L-canaline)進過中間物尿素型高絲氨酸(O-ureido-L-homoserine)形成的。這個反應途徑同尿素循環(Krebs-Henseleit ornithie-urea cycle)非常相似,刀豆氨酸在精氨酸酶的作用下分解為副刀豆氨酸和尿素。