基本介紹
- 藥品名稱:維思通?
- 藥品類型:處方藥、醫保工傷用藥
- 用途分類:其他抗精神病藥
成份,性狀,適應症,規格,用法用量,不良反應,禁忌,注意事項,孕婦及哺乳期婦女用藥,兒童用藥,老年用藥,藥物相互作用,藥物過量,藥理毒理,藥代動力學,貯藏,包裝,有效期,執行標準,生產企業,包裝企業,核准日期,修訂日期,
成份
活性成份:利培酮。
化學名稱:3-[2-[4-(6-氟-l,2-苯並異噁唑-3-基)-l-哌啶基]乙基]-6,7,8,9,-四氫-2-甲基-4H-吡啶並[1,2-α]嘧啶-4-酮。
化學結構式:
分子式:C23H27FN4O2
分子量:410.49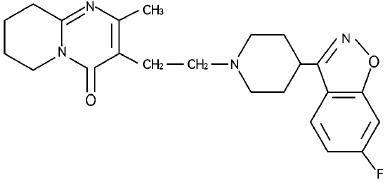
化學名稱:3-[2-[4-(6-氟-l,2-苯並異噁唑-3-基)-l-哌啶基]乙基]-6,7,8,9,-四氫-2-甲基-4H-吡啶並[1,2-α]嘧啶-4-酮。
化學結構式:
分子式:C23H27FN4O2
分子量:410.49

性狀
本品為無色的澄明液體。
適應症
1.用於治療急性和慢性精神分裂症以及其它各種精神病性狀態的明顯的陽性症狀(如幻覺、妄想、思維紊亂、敵視、懷疑)和明顯的陰性症狀(如反應遲鈍、情緒淡漠及社交淡漠、少語)。也可減輕與精神分裂症有關的情感症狀(如:抑鬱、負罪感、焦慮)。對於急性期治療有效的患者,在維持期治療中,本品可繼續發揮其臨床療效。
2.可用於治療雙相情感障礙的躁狂發作,其表現為情緒高漲、誇大或易激惹、自我評價過高、睡眠要求減少、語速加快、思維奔逸、注意力分散或判斷力低下(包括紊亂或過激行為)。
2.可用於治療雙相情感障礙的躁狂發作,其表現為情緒高漲、誇大或易激惹、自我評價過高、睡眠要求減少、語速加快、思維奔逸、注意力分散或判斷力低下(包括紊亂或過激行為)。
規格
(1)30ml:30mg (2)100ml:100mg。
用法用量
1、精神分裂症
由使用其他抗精神病藥改用本品者:開始使用時,應漸停原先使用的抗精神病藥。若病人原來使用的是長效抗精神病藥,則可用本品替換該藥治療。已用的抗帕金森氏綜合徵的藥是否需要繼續則應定期地進行再評定。
成人:每日1次或每日2次。
推薦起始劑量為一日二次,一次1mg,第二天增加到一日二次,一次2mg;如能耐受,第三天可增加到一日二次,每次3mg,此後,可維持此劑量不變,或根據個人情況進一步調整。
為期1-2年的臨床試驗表明利培酮延緩精神分裂症復發額有效劑量為2~8mg/天,同時也證實了採用一日一次給藥方式的有效性和安全性。試驗中起始劑量為第一日1mg,第二天增加到一日2mg,第三天可增加到一日4mg,此後,可維持次劑量不變或根據個人情況進一步調整。
臨床醫師應定期對患者進行再評估以確定用適當劑量進行維持治療的必要性。
不管採用何種給藥方式,對某些患者應進行緩慢的劑量調整,調整的間隔時間一般不少於一周;調整時,推薦增減劑量以1~2mg的小劑量進行。
利培酮的最大有效劑量範圍為每日4~8mg,但一日二次,每日劑量超過6mg給藥不能證明比較低劑量更有效,而且同更多的錐體外系症狀和其他副作用有關,因此一般不推薦使用。由於對劑量大於每日16mg的安全性尚未評定,因此每日用藥劑量不應超過16mg。
在需要加強鎮靜作用時,可加用苯二氮䓬類藥物。
2、治療雙相情感障礙的躁狂發作
推薦起始劑量每日1次,每次1~2mg,劑量可根據個體需要進行調整。劑量增加的幅度為每日1mg,劑量增加至少間隔24小時或間隔更多天數進行。大多數患者的理想劑量為每日2~6mg。在所有的對症治療期間,應不斷地對是否需要繼續使用本品進行評價。
3、肝腎功能損害的患者
腎功能損害患者清除抗精神病藥物的能力低於正常成人;而肝病患者血漿內利培酮未結合部分的濃度較正常值高。
腎病及肝病患者起始劑量及維持劑量均應減半,劑量調整幅度及速度應降低。建議起始劑量為每日二次,每次0.5mg。根據個體需要,劑量可逐漸加大到每日二次,每次1~2mg。劑量調整間隔應不小於1周,劑量增減的幅度為每日二次,每次0.5mg。這些患者的臨床套用經驗有限,用藥應謹慎。
服藥方法:
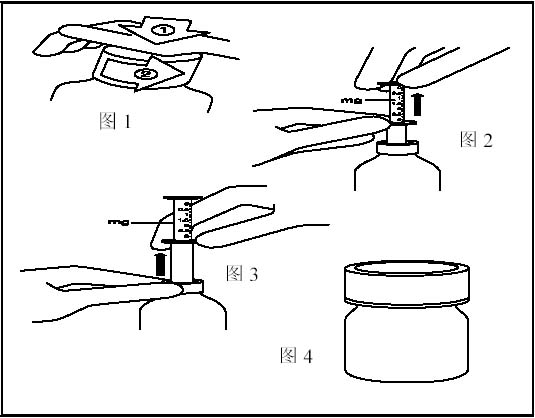
1、將藥瓶的瓶蓋下壓的同時逆時針旋轉,取下瓶蓋。(圖1)
2、將取樣器取出後插入已開蓋的藥瓶中。
3、握住取樣器下端的圓環,同時握住上端圓環向上拉出至所需服用藥量處。(圖2)
4、握住取樣器下端的圓環,將整個取樣器從藥瓶中取出。(圖3)
5、向下按取樣器上端圓環將其中口服液全部推入非酒精飲料中(茶水除外)。
6、擰緊藥瓶的瓶蓋。(圖4)
由使用其他抗精神病藥改用本品者:開始使用時,應漸停原先使用的抗精神病藥。若病人原來使用的是長效抗精神病藥,則可用本品替換該藥治療。已用的抗帕金森氏綜合徵的藥是否需要繼續則應定期地進行再評定。
成人:每日1次或每日2次。
推薦起始劑量為一日二次,一次1mg,第二天增加到一日二次,一次2mg;如能耐受,第三天可增加到一日二次,每次3mg,此後,可維持此劑量不變,或根據個人情況進一步調整。
為期1-2年的臨床試驗表明利培酮延緩精神分裂症復發額有效劑量為2~8mg/天,同時也證實了採用一日一次給藥方式的有效性和安全性。試驗中起始劑量為第一日1mg,第二天增加到一日2mg,第三天可增加到一日4mg,此後,可維持次劑量不變或根據個人情況進一步調整。
臨床醫師應定期對患者進行再評估以確定用適當劑量進行維持治療的必要性。
不管採用何種給藥方式,對某些患者應進行緩慢的劑量調整,調整的間隔時間一般不少於一周;調整時,推薦增減劑量以1~2mg的小劑量進行。
利培酮的最大有效劑量範圍為每日4~8mg,但一日二次,每日劑量超過6mg給藥不能證明比較低劑量更有效,而且同更多的錐體外系症狀和其他副作用有關,因此一般不推薦使用。由於對劑量大於每日16mg的安全性尚未評定,因此每日用藥劑量不應超過16mg。
在需要加強鎮靜作用時,可加用苯二氮䓬類藥物。
2、治療雙相情感障礙的躁狂發作
推薦起始劑量每日1次,每次1~2mg,劑量可根據個體需要進行調整。劑量增加的幅度為每日1mg,劑量增加至少間隔24小時或間隔更多天數進行。大多數患者的理想劑量為每日2~6mg。在所有的對症治療期間,應不斷地對是否需要繼續使用本品進行評價。
3、肝腎功能損害的患者
腎功能損害患者清除抗精神病藥物的能力低於正常成人;而肝病患者血漿內利培酮未結合部分的濃度較正常值高。
腎病及肝病患者起始劑量及維持劑量均應減半,劑量調整幅度及速度應降低。建議起始劑量為每日二次,每次0.5mg。根據個體需要,劑量可逐漸加大到每日二次,每次1~2mg。劑量調整間隔應不小於1周,劑量增減的幅度為每日二次,每次0.5mg。這些患者的臨床套用經驗有限,用藥應謹慎。
服藥方法:
1、將藥瓶的瓶蓋下壓的同時逆時針旋轉,取下瓶蓋。(圖1)
2、將取樣器取出後插入已開蓋的藥瓶中。
3、握住取樣器下端的圓環,同時握住上端圓環向上拉出至所需服用藥量處。(圖2)
4、握住取樣器下端的圓環,將整個取樣器從藥瓶中取出。(圖3)
5、向下按取樣器上端圓環將其中口服液全部推入非酒精飲料中(茶水除外)。
6、擰緊藥瓶的瓶蓋。(圖4)

不良反應
臨床試驗數據
在一項臨床試驗中評價本品的安全性,9712例不同類型的精神病患者(包括成人、老年痴呆患者和兒童)至少接受本品一個劑量的治療。其中2626例患者在參加雙盲、安慰劑對照試驗時接受了本品的治療。在治療狀況和持續時間上有很大的區別,包括雙盲、定量和不定量、安慰劑或活性對照試驗和開放期試驗的住院和門診患者,短期(至12周)和長期(至3年)給藥(交叉分類)。
多數不良反應為輕中度。
雙盲、安慰劑對照試驗——成年患者
在9項成年患者接受利培酮3至8周的雙盲、安慰劑對照試驗中,不少於1%的利培酮組患者報告的不良反應(ADRs)列於表1。
* 帕金森氏綜合徵包括錐體外系障礙、肌肉骨骼強直、帕金森氏綜合徵、齒輪樣強直、暫時性肌麻痹、運動徐緩、運動功能減退、面具臉、肌肉強直和帕金森氏病。靜坐不能包括靜坐不能和坐立不安。張力障礙包括張力障礙和肌肉痙攣、不自主肌收縮、肌肉攣縮、眼球旋動、舌肌麻痹。震顫包括震顫和帕金森氏病的休息性震顫。運動障礙包括運動障礙和肌肉顫搐、舞蹈病、舞蹈手足徐動症。
雙盲、安慰劑對照試驗——老年痴呆患者
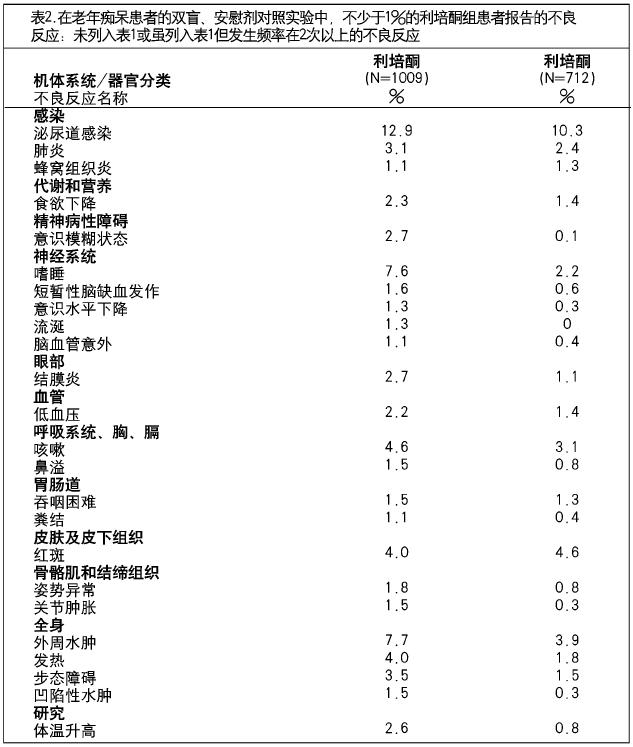
在6項老年痴呆患者接受利培酮4至12周的雙盲、安慰劑對照試驗中,不少於1%的利培酮組患者報告的不良反應列於表2。表2中只包括未列入表1或雖列入表1但發生頻率在2次及以上的不良反應。
雙盲、安慰劑對照試驗——兒童患者
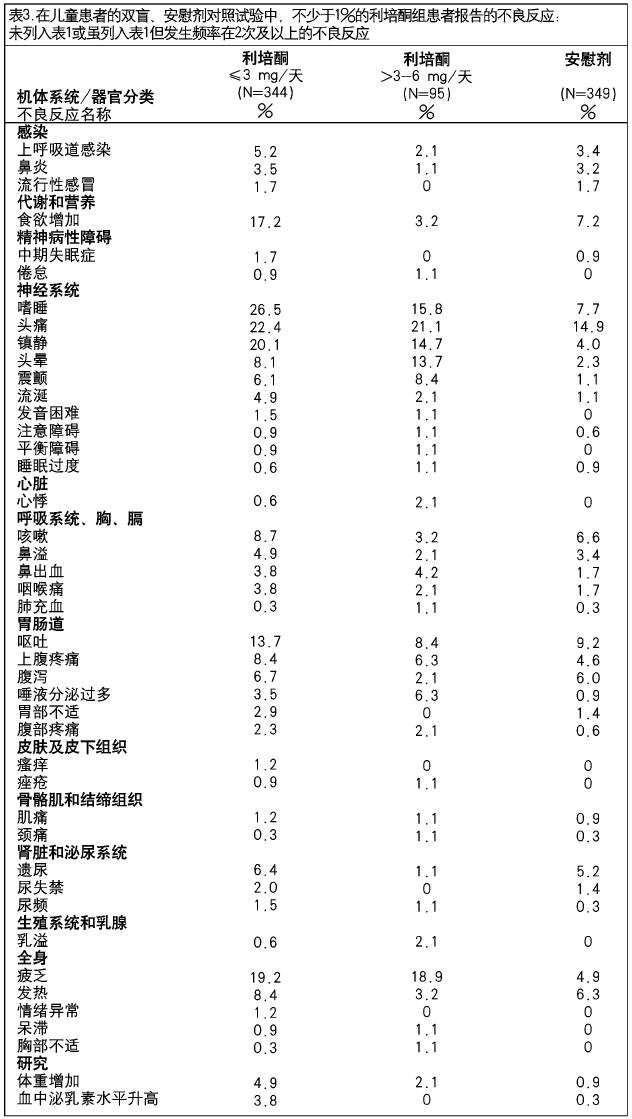
在8項兒童患者接受利培酮3至8周的雙盲、安慰劑對照試驗中,不少於1%的利培酮組患者報告的不良反應列於表3。表3中只包括未列入表1或雖列入表1但發生頻率在2次及以上的不良反應。
其它臨床試驗數據
在兒童、成年和老年痴呆患者的雙盲、安慰劑對照試驗中,少於1%的利培酮組患者報告的不良反應,或在雙盲、活性對照和開放期的其它試驗中,利培酮組患者報告的不良反應均列於表4。
報告自使用注射用利培酮微球的患者,與利培酮相關的其它不良反應如下,其中不包括與劑型或注射給藥途徑相關的不良反應。
感染:下呼吸道感染、感染、腸胃炎、皮下膿腫
血液和淋巴系統:嗜中性白血球減少症
精神病性障礙:抑鬱
神經系統:感覺異常、驚厥
眼部:瞼痙攣
耳部和迷路:眩暈
心臟:心動過緩
血管:高血壓
胃腸道:牙痛、舌痙攣
皮膚及皮下組織:濕疹
骨骼肌、結締組織和骨異常:臀痛
全身及給藥部位:疼痛
研究:體重下降、γ-谷氨酸轉移酶升高、肝酶水平升高
中毒和損傷:跌倒
上市後經驗
上市後首次判定為利培酮不良反應的不良事件見表5。不良反應按自發報告率分類:
很常見≥1/10
常見≥1/100,且1/10
少見≥1/1000,且<1/100
罕見≥1/10,000,且1/1000
非常罕見<1/10,000,包括個別病例。
依據自發報告頻率,以上不良反應按發生率分類列於表5。
a 包括血小板減少、血小板計數下降、血小板壓積減少、血小板產物減少
b 包括血管神經性水腫、後天性C1酯酶缺乏、口緣水腫、眼瞼浮腫、面部浮腫、遺傳性血管水腫、喉水腫、喉氣管水腫、眼-呼吸道綜合徵、口腔水腫、眶周水腫、小腸部血管性水腫、舌水腫
c 包括心電圖校正後的QT間期延長、心電圖QT間期異常、心電圖QT間期延長、QT間期延長綜合徵、先天性QT間期延長綜合徵。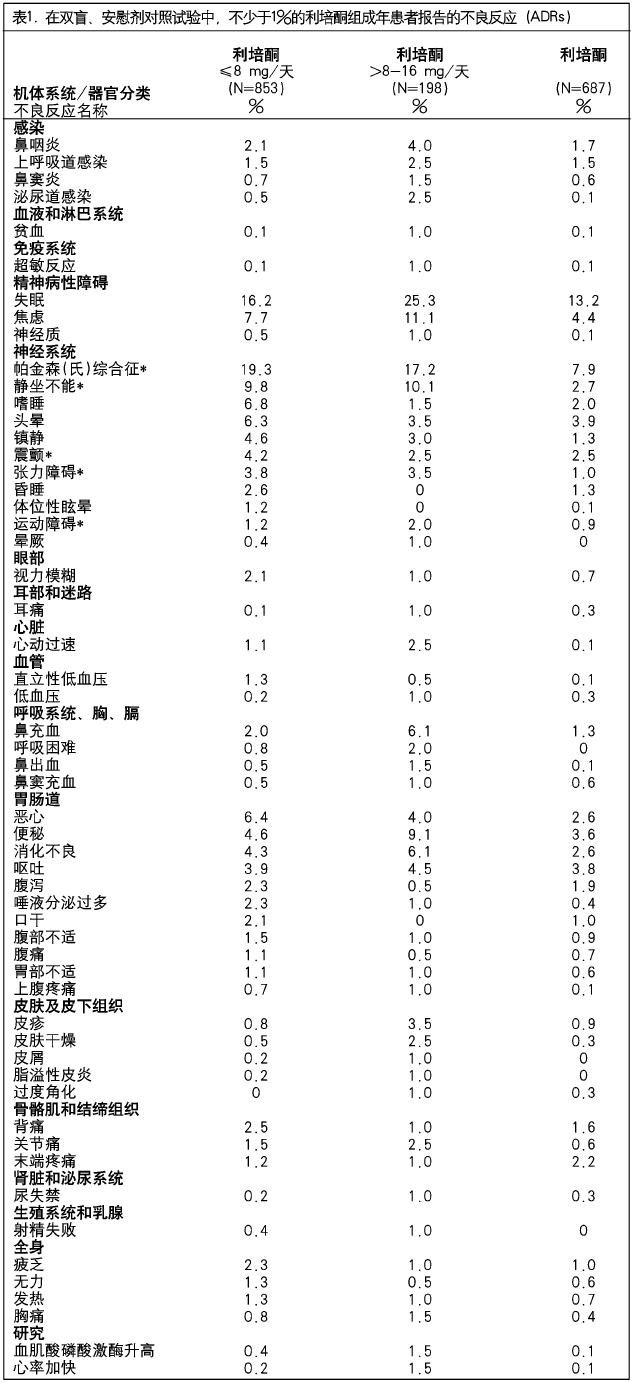


在一項臨床試驗中評價本品的安全性,9712例不同類型的精神病患者(包括成人、老年痴呆患者和兒童)至少接受本品一個劑量的治療。其中2626例患者在參加雙盲、安慰劑對照試驗時接受了本品的治療。在治療狀況和持續時間上有很大的區別,包括雙盲、定量和不定量、安慰劑或活性對照試驗和開放期試驗的住院和門診患者,短期(至12周)和長期(至3年)給藥(交叉分類)。
多數不良反應為輕中度。
雙盲、安慰劑對照試驗——成年患者
在9項成年患者接受利培酮3至8周的雙盲、安慰劑對照試驗中,不少於1%的利培酮組患者報告的不良反應(ADRs)列於表1。
* 帕金森氏綜合徵包括錐體外系障礙、肌肉骨骼強直、帕金森氏綜合徵、齒輪樣強直、暫時性肌麻痹、運動徐緩、運動功能減退、面具臉、肌肉強直和帕金森氏病。靜坐不能包括靜坐不能和坐立不安。張力障礙包括張力障礙和肌肉痙攣、不自主肌收縮、肌肉攣縮、眼球旋動、舌肌麻痹。震顫包括震顫和帕金森氏病的休息性震顫。運動障礙包括運動障礙和肌肉顫搐、舞蹈病、舞蹈手足徐動症。
雙盲、安慰劑對照試驗——老年痴呆患者
在6項老年痴呆患者接受利培酮4至12周的雙盲、安慰劑對照試驗中,不少於1%的利培酮組患者報告的不良反應列於表2。表2中只包括未列入表1或雖列入表1但發生頻率在2次及以上的不良反應。
雙盲、安慰劑對照試驗——兒童患者
在8項兒童患者接受利培酮3至8周的雙盲、安慰劑對照試驗中,不少於1%的利培酮組患者報告的不良反應列於表3。表3中只包括未列入表1或雖列入表1但發生頻率在2次及以上的不良反應。
其它臨床試驗數據
在兒童、成年和老年痴呆患者的雙盲、安慰劑對照試驗中,少於1%的利培酮組患者報告的不良反應,或在雙盲、活性對照和開放期的其它試驗中,利培酮組患者報告的不良反應均列於表4。
報告自使用注射用利培酮微球的患者,與利培酮相關的其它不良反應如下,其中不包括與劑型或注射給藥途徑相關的不良反應。
感染:下呼吸道感染、感染、腸胃炎、皮下膿腫
血液和淋巴系統:嗜中性白血球減少症
精神病性障礙:抑鬱
神經系統:感覺異常、驚厥
眼部:瞼痙攣
耳部和迷路:眩暈
心臟:心動過緩
血管:高血壓
胃腸道:牙痛、舌痙攣
皮膚及皮下組織:濕疹
骨骼肌、結締組織和骨異常:臀痛
全身及給藥部位:疼痛
研究:體重下降、γ-谷氨酸轉移酶升高、肝酶水平升高
中毒和損傷:跌倒
上市後經驗
上市後首次判定為利培酮不良反應的不良事件見表5。不良反應按自發報告率分類:
很常見≥1/10
常見≥1/100,且1/10
少見≥1/1000,且<1/100
罕見≥1/10,000,且1/1000
非常罕見<1/10,000,包括個別病例。
依據自發報告頻率,以上不良反應按發生率分類列於表5。
a 包括血小板減少、血小板計數下降、血小板壓積減少、血小板產物減少
b 包括血管神經性水腫、後天性C1酯酶缺乏、口緣水腫、眼瞼浮腫、面部浮腫、遺傳性血管水腫、喉水腫、喉氣管水腫、眼-呼吸道綜合徵、口腔水腫、眶周水腫、小腸部血管性水腫、舌水腫
c 包括心電圖校正後的QT間期延長、心電圖QT間期異常、心電圖QT間期延長、QT間期延長綜合徵、先天性QT間期延長綜合徵。





禁忌
已知對本品過敏的患者禁用。
注意事項
1. 老年痴呆患者
總死亡率
對包括本品在內的幾個非典型抗精神病藥進行的17項對照試驗匯總分析結果顯示,非典型抗精神病藥物組老年痴呆患者的死亡率較安慰劑組有所增加。在對此類人群用本品進行的安慰劑對照試驗中,本品組和安慰劑組患者的死亡率分別為4.0%和3.1%。死亡患者的平均年齡為86歲(範圍在67~100歲之間)。
與呋塞米合用
在對老年痴呆患者用本品進行的安慰劑對照研究中,利培酮與呋塞米合併用藥患者的死亡率高於單獨使用利培酮或呋塞米的患者,分別為7.3%(平均年齡89歲,範圍75-97歲)、3.1%(平均年齡84歲,範圍70-96歲)和4.1%(平均年齡80歲,範圍67-90歲)。在4項臨床試驗中的2項觀察到了合用呋塞米和本品的患者死亡率增加的現象。
儘管尚未找到明確的病理生理學機制來解釋這一現象,並且患者的死亡原因也不相同,但對老年患者合併給利培酮和呋塞米時需謹慎評估風險利益。在服用利培酮併合用其它利尿劑的患者中,並未出現以上死亡率增加的現象。由於脫水是老年痴呆患者很重要的致死因素,所以應儘量避免脫水的發生。
2. 腦血管意外(CAE)
在對老年痴呆患者(平均年齡85歲,範圍73-97歲)進行的安慰劑對照研究中,觀察到利培酮組包括死亡在內的腦血管方面不良事件(腦血管意外和短暫性腦缺血發作)的發生率較安慰劑組高。
3. 對α受體的阻斷活性
由於本品具有對α受體的阻斷作用,可能會發生(體位性)低血壓,尤其是在治療初期的劑量調整階段。對於已知患有心血管疾病的患者(如心衰、心肌梗塞、傳導異常、脫水、血容量降低或腦血管疾病)應慎用本品,劑量應按推薦劑量逐漸增加(見用法用量),如發生血壓過低現象,應考慮減少劑量。
4. 遲發性運動障礙/錐體外系症狀(TD/EPS)
同其它所有具有多巴胺受體拮抗劑性質的藥物相似,本品也可能引起遲發性運動障礙,其特徵為有節律的非自主運動,主要見於舌及面部。有報告表明,錐體外系症狀的發生是遲發性運動障礙發展的風險因素,而與其它傳統抗精神病藥物相比,本品較少引起錐體外系症狀,因此與傳統抗精神病藥物相比,本品引發遲發性運動障礙的風險較低。如果出現遲發性運動障礙的症狀,應考慮停用所有的抗精神病藥。
5. 抗精神病藥的惡性綜合徵(NMS)
已有報告指出,服用傳統的抗精神病藥可能會出現惡性綜合徵,其特徵為高熱、肌肉僵直、顫抖、意識障礙和血清肌酸磷酸激酶水平升高,還可能出現肌紅蛋白尿症(橫紋肌溶解症)和急性腎衰。此時應停用包括本品在內的所有抗精神病藥物。
對於路易氏小體性痴呆或帕金森氏病患者,在處方抗精神病藥(包括本品)時,應權衡利弊,這類藥物可能增加惡性綜合徵的風險。同時以上人群對抗精神病藥物的敏感度增加,除出現錐體外系症狀外還會出現混亂、遲鈍、體位不穩而經常跌倒。
6. 高血糖
罕見高血糖及原有糖尿病加重的報告。糖尿病患者及糖尿病高危人群服用本品時應進行適當的臨床監測。
7. QT間期
與其它抗精神病藥物一樣,對有心律失常病史、先天性QT間期延長綜合徵的患者給予本品,及與已知會延長QT間期的藥物合用時,應謹慎。
8. 其它
傳統的抗精神病藥會減低癲癇的發作閾值,故癲癇患者應慎用本品。
服用本品的患者應避免進食過多,因為本品可能引起體重增加。
對於老年患者、肝功能損害患者、腎功能損害患者或老年痴呆患者推薦的特殊劑量,參見[老年用藥]和[用法用量]部分。
本品對需要警覺性的活動有所影響。因此,在了解到患者對本品的敏感性前,建議患者在治療期間不應駕駛汽車或操作機器。
請置於兒童不易拿到處。
總死亡率
對包括本品在內的幾個非典型抗精神病藥進行的17項對照試驗匯總分析結果顯示,非典型抗精神病藥物組老年痴呆患者的死亡率較安慰劑組有所增加。在對此類人群用本品進行的安慰劑對照試驗中,本品組和安慰劑組患者的死亡率分別為4.0%和3.1%。死亡患者的平均年齡為86歲(範圍在67~100歲之間)。
與呋塞米合用
在對老年痴呆患者用本品進行的安慰劑對照研究中,利培酮與呋塞米合併用藥患者的死亡率高於單獨使用利培酮或呋塞米的患者,分別為7.3%(平均年齡89歲,範圍75-97歲)、3.1%(平均年齡84歲,範圍70-96歲)和4.1%(平均年齡80歲,範圍67-90歲)。在4項臨床試驗中的2項觀察到了合用呋塞米和本品的患者死亡率增加的現象。
儘管尚未找到明確的病理生理學機制來解釋這一現象,並且患者的死亡原因也不相同,但對老年患者合併給利培酮和呋塞米時需謹慎評估風險利益。在服用利培酮併合用其它利尿劑的患者中,並未出現以上死亡率增加的現象。由於脫水是老年痴呆患者很重要的致死因素,所以應儘量避免脫水的發生。
2. 腦血管意外(CAE)
在對老年痴呆患者(平均年齡85歲,範圍73-97歲)進行的安慰劑對照研究中,觀察到利培酮組包括死亡在內的腦血管方面不良事件(腦血管意外和短暫性腦缺血發作)的發生率較安慰劑組高。
3. 對α受體的阻斷活性
由於本品具有對α受體的阻斷作用,可能會發生(體位性)低血壓,尤其是在治療初期的劑量調整階段。對於已知患有心血管疾病的患者(如心衰、心肌梗塞、傳導異常、脫水、血容量降低或腦血管疾病)應慎用本品,劑量應按推薦劑量逐漸增加(見用法用量),如發生血壓過低現象,應考慮減少劑量。
4. 遲發性運動障礙/錐體外系症狀(TD/EPS)
同其它所有具有多巴胺受體拮抗劑性質的藥物相似,本品也可能引起遲發性運動障礙,其特徵為有節律的非自主運動,主要見於舌及面部。有報告表明,錐體外系症狀的發生是遲發性運動障礙發展的風險因素,而與其它傳統抗精神病藥物相比,本品較少引起錐體外系症狀,因此與傳統抗精神病藥物相比,本品引發遲發性運動障礙的風險較低。如果出現遲發性運動障礙的症狀,應考慮停用所有的抗精神病藥。
5. 抗精神病藥的惡性綜合徵(NMS)
已有報告指出,服用傳統的抗精神病藥可能會出現惡性綜合徵,其特徵為高熱、肌肉僵直、顫抖、意識障礙和血清肌酸磷酸激酶水平升高,還可能出現肌紅蛋白尿症(橫紋肌溶解症)和急性腎衰。此時應停用包括本品在內的所有抗精神病藥物。
對於路易氏小體性痴呆或帕金森氏病患者,在處方抗精神病藥(包括本品)時,應權衡利弊,這類藥物可能增加惡性綜合徵的風險。同時以上人群對抗精神病藥物的敏感度增加,除出現錐體外系症狀外還會出現混亂、遲鈍、體位不穩而經常跌倒。
6. 高血糖
罕見高血糖及原有糖尿病加重的報告。糖尿病患者及糖尿病高危人群服用本品時應進行適當的臨床監測。
7. QT間期
與其它抗精神病藥物一樣,對有心律失常病史、先天性QT間期延長綜合徵的患者給予本品,及與已知會延長QT間期的藥物合用時,應謹慎。
8. 其它
傳統的抗精神病藥會減低癲癇的發作閾值,故癲癇患者應慎用本品。
服用本品的患者應避免進食過多,因為本品可能引起體重增加。
對於老年患者、肝功能損害患者、腎功能損害患者或老年痴呆患者推薦的特殊劑量,參見[老年用藥]和[用法用量]部分。
本品對需要警覺性的活動有所影響。因此,在了解到患者對本品的敏感性前,建議患者在治療期間不應駕駛汽車或操作機器。
請置於兒童不易拿到處。
孕婦及哺乳期婦女用藥
懷孕婦女服用本品是否安全尚不明確。動物試驗表明:利培酮對生殖無直接的毒性,但曾觀察到一些間接的與催乳素及中樞神經相關的作用。本品無致畸作用,但孕婦服用本品應權衡利弊。
動物試驗表明,利培酮和9-羥基利培酮會經動物乳汁排出。同時,人體試驗也已證明本品會經母乳排出,因此,服用本品的婦女不應哺乳。
動物試驗表明,利培酮和9-羥基利培酮會經動物乳汁排出。同時,人體試驗也已證明本品會經母乳排出,因此,服用本品的婦女不應哺乳。
兒童用藥
對於精神分裂症,目前尚缺乏15歲以下兒童的足夠的臨床經驗。
對於品行障礙和其它行為紊亂,目前尚缺乏5歲以下兒童的足夠的臨床經驗。
對於雙相情感障礙的狂躁發作,目前尚缺乏18歲以下兒童及青少年的足夠臨床經驗。
對於品行障礙和其它行為紊亂,目前尚缺乏5歲以下兒童的足夠的臨床經驗。
對於雙相情感障礙的狂躁發作,目前尚缺乏18歲以下兒童及青少年的足夠臨床經驗。
老年用藥
治療精神分裂症:建議起始劑量為每次0.5mg、每日2次,劑量可根據個體需要進行調整。劑量增加的幅度為每次0.5mg、每日2次,直至一次1~2mg、每日2次。
藥物相互作用
1.鑒於本品對中樞神經系統的作用,在與其它作用於中樞系統的藥物合用時應慎重。
2.本品可拮抗左旋多巴及其它多巴胺激動劑的作用。
3.上市後合用抗高血壓藥物時,曾觀察到有臨床意義的低血壓。
4.與已知會延長QT間期的藥物合用時應謹慎。
5.卡馬西平及其它CYP 3A4肝酶誘導劑會降低本品活性成份的血漿濃度,開始或停止使用卡馬西平或其它CYP 3A4肝酶誘導劑時,應重新確定使用本品的劑量。
6.氟西汀和帕羅西汀(CYP2D6抑制劑)可增加本品的血藥濃度,但對其抗精神病活性成份血藥濃度的影響較小。當開始或停止與氟西汀或帕羅西汀合用時,醫生應重新確定本品的劑量。
7.托吡酯略降低利培酮的生物利用度,對本品中的抗精神病活性成份無影響。因此,該相互作用基本上不具有臨床意義。
8.酚噻嗪類抗精神病藥、三環抗抑鬱藥和一些β-阻斷劑會增加本品的血藥濃度,但不增加其抗精神病活性成份的血藥濃度。阿米替林不影響利培酮或其抗精神病活性成份的藥代動力學參數。西咪替丁和雷尼替丁可增加利培酮的生物利用度,但對其抗精神病活性成份的影響很小。紅黴素(CYP3A4抑制劑)不影響利培酮或其抗精神病活性成份的藥代動力學參數。膽鹼酯酶抑制劑加蘭他敏和多奈哌齊對利培酮或其抗精神病活性成份的藥代動力學參數無顯著影響。
9.當和其它高度蛋白結合的藥物一起服用時,不存在有臨床意義的血漿蛋白的相互置換。
10.本品對鋰、丙戊酸鈉、地高辛或托吡酯的藥代動力學參數無顯著影響。
11.有關老年痴呆患者合用呋塞米治療死亡率增加的內容參見【注意事項】部分。
12.食物不影響本品的吸收。
2.本品可拮抗左旋多巴及其它多巴胺激動劑的作用。
3.上市後合用抗高血壓藥物時,曾觀察到有臨床意義的低血壓。
4.與已知會延長QT間期的藥物合用時應謹慎。
5.卡馬西平及其它CYP 3A4肝酶誘導劑會降低本品活性成份的血漿濃度,開始或停止使用卡馬西平或其它CYP 3A4肝酶誘導劑時,應重新確定使用本品的劑量。
6.氟西汀和帕羅西汀(CYP2D6抑制劑)可增加本品的血藥濃度,但對其抗精神病活性成份血藥濃度的影響較小。當開始或停止與氟西汀或帕羅西汀合用時,醫生應重新確定本品的劑量。
7.托吡酯略降低利培酮的生物利用度,對本品中的抗精神病活性成份無影響。因此,該相互作用基本上不具有臨床意義。
8.酚噻嗪類抗精神病藥、三環抗抑鬱藥和一些β-阻斷劑會增加本品的血藥濃度,但不增加其抗精神病活性成份的血藥濃度。阿米替林不影響利培酮或其抗精神病活性成份的藥代動力學參數。西咪替丁和雷尼替丁可增加利培酮的生物利用度,但對其抗精神病活性成份的影響很小。紅黴素(CYP3A4抑制劑)不影響利培酮或其抗精神病活性成份的藥代動力學參數。膽鹼酯酶抑制劑加蘭他敏和多奈哌齊對利培酮或其抗精神病活性成份的藥代動力學參數無顯著影響。
9.當和其它高度蛋白結合的藥物一起服用時,不存在有臨床意義的血漿蛋白的相互置換。
10.本品對鋰、丙戊酸鈉、地高辛或托吡酯的藥代動力學參數無顯著影響。
11.有關老年痴呆患者合用呋塞米治療死亡率增加的內容參見【注意事項】部分。
12.食物不影響本品的吸收。
藥物過量
出現急性過量症狀時,應考慮是否有其它藥物合用引起的因素。
一般來說,所報導的過量時的症狀和體徵均為其藥理作用的延伸所致,包括嗜睡和鎮靜、心動過速和低血壓、以及錐體外系症狀。藥物過量時,曾有QT間期延長和癲癇的報告。過量的本品合用帕羅西汀時,曾有扭轉型室性心動過速的報告。
過量解救時,應維持氣道的通暢,確保足夠的氧氣和良好的通氣,且應考慮洗胃(若患者意識喪失應插管進行)及給予活性炭和輕瀉劑,並應立即進行心血管監測,其中包括連續的心電圖監測,以發現可能出現的心律失常。本品無特定的解救藥。因此,應採用適當的支持療法。對低血壓及循環衰竭可採用靜脈輸液,或給予擬交感神經藥等適當措施加以糾正.一旦出現嚴重的錐體外系症狀時,則應給予抗膽鹼藥,在病人恢復前應持續進行密切的醫療監測及監護。
一般來說,所報導的過量時的症狀和體徵均為其藥理作用的延伸所致,包括嗜睡和鎮靜、心動過速和低血壓、以及錐體外系症狀。藥物過量時,曾有QT間期延長和癲癇的報告。過量的本品合用帕羅西汀時,曾有扭轉型室性心動過速的報告。
過量解救時,應維持氣道的通暢,確保足夠的氧氣和良好的通氣,且應考慮洗胃(若患者意識喪失應插管進行)及給予活性炭和輕瀉劑,並應立即進行心血管監測,其中包括連續的心電圖監測,以發現可能出現的心律失常。本品無特定的解救藥。因此,應採用適當的支持療法。對低血壓及循環衰竭可採用靜脈輸液,或給予擬交感神經藥等適當措施加以糾正.一旦出現嚴重的錐體外系症狀時,則應給予抗膽鹼藥,在病人恢復前應持續進行密切的醫療監測及監護。
藥理毒理
1.藥理作用
利培酮是一種選擇性的單胺能拮抗劑,對5HT2受體、D2受體、α1及α2受體和H1受體親和力高。對其它受體亦有拮抗作用,但較弱。對5HT1C,5HT1D和5HT1A有低到中度的親和力,對D1及氟哌啶醇敏感的σ受體親和力弱,對M受體或β1及β2受體沒有親和作用。
與其它治療精神分裂症的藥物一樣,利培酮治療精神分裂症的機制尚不清楚。據認為其治療作用是對D2受體及5HT2受體拮抗聯合效應的結果。對D2及5HT2以外其它受體的拮抗作用可能與利培酮的其它作用有關。
2.毒理研究
遺傳毒性:Ames逆向突變試驗、小鼠淋巴細胞畸變試驗、體外大鼠肝細胞DNA修複試驗、小鼠體內微核試驗、果蠅性別相關隱性致死試驗、人淋巴細胞或中國倉鼠細胞染色體畸變試驗均未發現利培酮有潛在致突變性。
生殖毒性:在Wistar大鼠的生殖毒性研究中,利培酮0.16~5mg/kg(以mg/m[sup]2[/sup]計,為人最大推薦劑量的0.16~4.9倍,人用最大推薦劑量為10mg/日,見用法用量部分)降低交配次數,但不影響生育力。該影響只發生在雌性大鼠上,在只給予雄性大鼠藥物處理的一般生殖毒性試驗中未觀察到交配行為受影響。Beagle犬的亞慢性研究中,利培酮劑量為0.31~5mg/kg(以mg/m[sup]2[/sup]計,為人最大推薦劑量的1.0~16.2倍)時,精子活力及濃度下降,相同劑量下血清睪酮水平劑量相關性降低。停藥後,血清睪酮水平及精子參數可部分恢復,但仍處於低水平。大鼠或犬均沒有觀察到無影響劑量。
在SD及Wistar大鼠和紐西蘭家兔上進行了利培酮劑量分別為0.63~10mg/kg,0.31~5mg/kg(以mg/m[sup]2[/sup]計,分別為人最大推薦劑量的0.6~6倍和0.4~6倍)的致畸作用研究。與對照組比較,未觀察到畸形發生率增加。劑量在0.16~5mg/kg(以mg/m[sup]2[/sup]計,分別為人最大推薦劑量的0.16~4.9倍)時,大鼠哺乳期前4天幼仔死亡增加。尚不知這些死亡是由於對胎仔或幼仔的直接作用,還是對母鼠的影響造成。
沒有觀察到引發大鼠幼仔死亡率增加的無影響劑量。一項圍產期生殖毒性研究中,2.5mg/kg(以mg/m[sup]2[/sup]計,人最大推薦劑量的2.4倍)時,大鼠幼仔死產增加。在一項大鼠交叉撫養研究中.對胎仔或幼仔的毒性作用表現為出生時活幼仔數減少、死幼仔數增加、與母鼠給藥量相關的幼仔出生體重降低。此外,還有與母鼠給藥量相關的幼仔出生第一天死亡增加,無論幼仔是否交叉撫養。利培酮對母體行為可能有損害,由對照動物生產而由給藥母鼠撫養幼仔的體重增加量和生存率降低(哺乳第1~4天)。這些作用均在5mg/kg(以mg/m[sup]2[/sup]計,人最大推薦劑量的4.9倍)劑量組中觀察到。
利培酮可通過胎盤轉運至大鼠幼仔體內。
致癌性:小鼠、大鼠摻食法分別給予利培酮0.63、2.5和10mg/kg(以mg/kg計,分別為人最大推薦劑量的3.8、15、60倍,小鼠以mg/m[sup]2[/sup]計,分別為人最大推薦劑量的0.3、1.2、4.9倍,大鼠以mg/m[sup]2[/sup]計,分別為人最大推薦劑量的0.6、2.4、9.8倍),給藥周期分別為18個月和25個月。雄性小鼠未達最大耐受劑量。結果顯示,垂體腺瘤、內分泌性胰腺腺瘤和乳腺腺癌出現有統計學意義的顯著增加。抗精神病藥物可使嚙齒類動物催乳素水平長期升高。在利培酮致癌性試驗中沒有測定催乳素水平,但在亞慢性毒性研究中的測定結果顯示,與致癌性試驗中相同的利培酮劑量可使小鼠和大鼠的催乳素水平升高5到6倍。其它抗精神病藥物長期給藥時,在嚙齒類動物中發現乳腺、垂體及胰腺腫瘤發生增加,並認為是由催乳素介導。在嚙齒類動物上催乳素介導的內分泌腫瘤的發生與人用風險的相關性尚不清楚。
利培酮是一種選擇性的單胺能拮抗劑,對5HT2受體、D2受體、α1及α2受體和H1受體親和力高。對其它受體亦有拮抗作用,但較弱。對5HT1C,5HT1D和5HT1A有低到中度的親和力,對D1及氟哌啶醇敏感的σ受體親和力弱,對M受體或β1及β2受體沒有親和作用。
與其它治療精神分裂症的藥物一樣,利培酮治療精神分裂症的機制尚不清楚。據認為其治療作用是對D2受體及5HT2受體拮抗聯合效應的結果。對D2及5HT2以外其它受體的拮抗作用可能與利培酮的其它作用有關。
2.毒理研究
遺傳毒性:Ames逆向突變試驗、小鼠淋巴細胞畸變試驗、體外大鼠肝細胞DNA修複試驗、小鼠體內微核試驗、果蠅性別相關隱性致死試驗、人淋巴細胞或中國倉鼠細胞染色體畸變試驗均未發現利培酮有潛在致突變性。
生殖毒性:在Wistar大鼠的生殖毒性研究中,利培酮0.16~5mg/kg(以mg/m[sup]2[/sup]計,為人最大推薦劑量的0.16~4.9倍,人用最大推薦劑量為10mg/日,見用法用量部分)降低交配次數,但不影響生育力。該影響只發生在雌性大鼠上,在只給予雄性大鼠藥物處理的一般生殖毒性試驗中未觀察到交配行為受影響。Beagle犬的亞慢性研究中,利培酮劑量為0.31~5mg/kg(以mg/m[sup]2[/sup]計,為人最大推薦劑量的1.0~16.2倍)時,精子活力及濃度下降,相同劑量下血清睪酮水平劑量相關性降低。停藥後,血清睪酮水平及精子參數可部分恢復,但仍處於低水平。大鼠或犬均沒有觀察到無影響劑量。
在SD及Wistar大鼠和紐西蘭家兔上進行了利培酮劑量分別為0.63~10mg/kg,0.31~5mg/kg(以mg/m[sup]2[/sup]計,分別為人最大推薦劑量的0.6~6倍和0.4~6倍)的致畸作用研究。與對照組比較,未觀察到畸形發生率增加。劑量在0.16~5mg/kg(以mg/m[sup]2[/sup]計,分別為人最大推薦劑量的0.16~4.9倍)時,大鼠哺乳期前4天幼仔死亡增加。尚不知這些死亡是由於對胎仔或幼仔的直接作用,還是對母鼠的影響造成。
沒有觀察到引發大鼠幼仔死亡率增加的無影響劑量。一項圍產期生殖毒性研究中,2.5mg/kg(以mg/m[sup]2[/sup]計,人最大推薦劑量的2.4倍)時,大鼠幼仔死產增加。在一項大鼠交叉撫養研究中.對胎仔或幼仔的毒性作用表現為出生時活幼仔數減少、死幼仔數增加、與母鼠給藥量相關的幼仔出生體重降低。此外,還有與母鼠給藥量相關的幼仔出生第一天死亡增加,無論幼仔是否交叉撫養。利培酮對母體行為可能有損害,由對照動物生產而由給藥母鼠撫養幼仔的體重增加量和生存率降低(哺乳第1~4天)。這些作用均在5mg/kg(以mg/m[sup]2[/sup]計,人最大推薦劑量的4.9倍)劑量組中觀察到。
利培酮可通過胎盤轉運至大鼠幼仔體內。
致癌性:小鼠、大鼠摻食法分別給予利培酮0.63、2.5和10mg/kg(以mg/kg計,分別為人最大推薦劑量的3.8、15、60倍,小鼠以mg/m[sup]2[/sup]計,分別為人最大推薦劑量的0.3、1.2、4.9倍,大鼠以mg/m[sup]2[/sup]計,分別為人最大推薦劑量的0.6、2.4、9.8倍),給藥周期分別為18個月和25個月。雄性小鼠未達最大耐受劑量。結果顯示,垂體腺瘤、內分泌性胰腺腺瘤和乳腺腺癌出現有統計學意義的顯著增加。抗精神病藥物可使嚙齒類動物催乳素水平長期升高。在利培酮致癌性試驗中沒有測定催乳素水平,但在亞慢性毒性研究中的測定結果顯示,與致癌性試驗中相同的利培酮劑量可使小鼠和大鼠的催乳素水平升高5到6倍。其它抗精神病藥物長期給藥時,在嚙齒類動物中發現乳腺、垂體及胰腺腫瘤發生增加,並認為是由催乳素介導。在嚙齒類動物上催乳素介導的內分泌腫瘤的發生與人用風險的相關性尚不清楚。
藥代動力學
利培酮經口服後可被完全吸收,並在1~2小時內達到血藥濃度峰值,其吸收不受食物影響,因此可單獨服用或與食物同服。在體內,利培酮經CYP2D6代謝成9-羥基利培酮,後者與利培酮有相似的藥理作用。利培酮與9-羥基利培酮共同構成本品抗精神病有效成份,利培酮在體內的另外一個代謝途徑為N-脫烴作用。利培酮的消除半衰期為3小時左右,9-羥基利培酮及其它活性代謝物消除半衰期均為24小時。大多數病人在1天內達到利培酮的穩態,經過4~5天達到9-羥基利培酮的穩態,在治療劑量範圍內,利培酮的血藥濃度與給藥劑量成正比。用藥一周后,70%的藥物經尿液排泄,14%的藥物經糞便排出,經尿排泄的部分中,35~45%為利培酮和9-羥基利培酮,其餘為非活性代謝物。一項單劑量研究顯示,老年患者和腎功能不全患者的本品活性成份血漿濃度較高,活性成份的清除率在老年患者體內下降30%,在腎功能不全患者體內下降60%。利培酮血漿濃度在肝功能不全患者中正常,但是血漿中利培酮未結合部分平均增加約35%。利培酮、9-羥基利培酮及其它活性代謝物在兒童體內的藥代動力學與成人相似。
貯藏
15~30℃保存,勿冷凍。
包裝
帶白色聚丙烯蓋的琥珀色玻璃瓶,30ml/瓶,100ml/瓶。
有效期
36個月。
執行標準
JX20010091
生產企業
比利時楊森製藥公司
包裝企業
西安楊森製藥有限公司
核准日期
2006年09月12日
修訂日期
2007年02月20日 2007年03月09日 2007年12月30日 2008年04月29日
