簡介
普通外科學是
臨床外科學根據治療目標的不同而分工的一種(現專指各種腹腔、乳房、甲狀腺及簡單的皮膚外科)。學科研究範圍:普外科的學科研究範圍包括總論及各論兩部分:總論:水、電解質與酸鹼平衡,休克,多器官功能衰竭,外科營養,外科免疫,外科感染及器官移植等。各論:甲狀腺、乳房、胃腸、肝、膽、胰、脾等器宮組織的各種疾病及周圍血管疾病的診斷及治療。研究方式:動物實驗或臨床研究。
胰腺移植術
移植手術
世界上第一例胰腺移植(pancreas transplantation)由美國明尼蘇達州立大學的Kelly和Lillehei於1966年完成。該手術的成功使得許多胰島素依賴型糖尿病(IDDM)患者得到了有效的治療。據推測至2010年全球糖尿病患者預計將超過3.5億,其中5%~10%的患者將因糖尿病晚期出現的糖尿病腎病、視網膜病變、微血管病變和神經末梢病變等併發症而直接影響生命。胰腺移植能增加患者胰島素分泌細胞,從而有效地控制血糖,防止和改善糖尿病的併發症,提高生活質量,是治療IDDM的有效手段。目前該手術已被
美國糖尿病協會接受為1型糖尿病合併終末期腎病(ESRD)的標準治療方法。據國際胰腺移植登記中心(IPTR)記錄,截至2006年5月全世界共報導胰腺移植手術24000餘例。1989年同濟醫科大學器官移植所開展國內首例胰腎聯合移植以來,至2005年已有20多個單位施行胰腎聯合移植。
 普通外科學
普通外科學適應證
ESRD是胰腺移植的標準適應證,約占移植總數的94%。從理論上講,為了將糖尿病相關併發症的危害控制到最低,減輕長期治療下的昂貴經濟負擔,所有1型糖尿病患者均適宜於胰腺移植。對於
糖尿病腎病,美國移植中心建議,當肌酐清除率(CCr)<40ml/min時實施胰腎聯合移植(SPK);而在歐洲,基於對器官短缺等因素的考慮,大多數移植中心較嚴格地將CCr<20ml/min的患者列入胰腺移植的輪候名單。Sollinger在1999年提出的適應證為:(1)腎衰竭(進展期糖尿病腎病或依賴於透析治療,血肌酐>3mg/dl);(2)血清C肽濃度下降;(3)較低的心血管疾病風險[沒有或輕微的冠心病(運動實驗陰性)];(4)無糖尿病血管併發症,如截肢等;(5)有良好的對PT的心理順應性;(6)能很好理解PT的複雜性,並能遵從移植後治療方案。
SPK治療2型糖尿病合併終末期腎病一度存在較大爭議,但其成功病例不乏見報導,近年來,2型糖尿病接受胰腺移植的患者呈增多趨勢。2001年2型糖尿病也被美國器官分享網路(UNOS)正式列為適應證之一。
手術方式
胰腺移植主要包括單獨胰腺移植(pancreas transplantation alone,PTA)、腎移植後胰腺移植(pancreas after kidney transplantation,PAK)和胰腎聯合移植(simultaneous pancreas?kidney transplantation,SPK)。SPK適用於患尿毒症或終末期前腎病(CCr<50ml/min)的糖尿病患者。通常胰和腎移植物來自同一個屍體供者,但也可以是屍體全胰和活體腎移植或活體節段胰和腎移植。在SPK受者中HLA的配型對移植胰的存活率的影響不是很大,但在
PTA中
HLA配型卻顯得很重要。SPK的優點還包括同時糾正了糖代謝紊亂和尿毒症;胰腎取自同一供體,抗原單一;只需一次手術和一次大劑量免疫抑制劑治療;移植胰的早期排斥反應可通過移植腎來監測;胰腎免疫保護作用和移植成功率高,移植胰的1年存活率為83%。SPK阻止了移植腎糖尿病腎病的復發,移植腎存活率較單純腎移植高,所以全世界迄今為止已實施的胰腺移植中約90%採用該術式。PAK是患者先前接受了腎移植(屍體或活體來源)後再移植胰腺,其胰腺和腎移植物分別來自2個供者。PTA受者一般是患尿毒症前的型糖尿病患者,這些
患者的糖尿病併發症(增殖型糖尿病視網膜病、自發性糖尿病腎病和微蛋白尿)通常發展很快,呈進行性惡化,且易頻繁發生低血糖性昏迷,故胰腺移植對他們來說雖然會出現長期免疫抑制治療的不良反應,但其生活質量還是明顯改善了。
免疫抑制劑
免疫抑制劑是一類在腫瘤化療、器官移植、免疫病理學和臨床免疫學等多學科研究基礎上發展起來的新的藥劑類別,具有免疫抑制作用,可抑制機體異常的免疫反應,目前廣泛套用於器官移植抗排斥反應和自身免疫性疾病的治療。此類藥物已經歷了將近百年發展。百年來,人類在與病魔作鬥爭的過程中,一直在苦苦尋覓著療效好、使用安全的藥物。醫學研究者們對免疫抑制藥物的不斷探索與研究,新型藥物的不斷問世,使免疫抑制藥物在臨床中的套用占有越來越重要的地位。
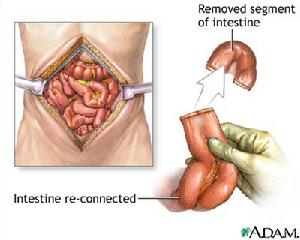 普通外科學
普通外科學環磷醯胺
(cyclophosphamide,CTX)最早套用於臨床,後來人們發現它在體內可被肝細胞微粒體羥化,產生具有烷化作用的代謝產物而具有強而持久的免疫作用。它通過殺傷免疫細胞,影響免疫過程中的各階段,作為一種免疫抑制劑用於
腎病綜合徵、
系統性紅斑狼瘡、類風濕關節炎等。較明顯的副作用使其套用受到了限制。1949年,Edward與Philip經過不懈努力,終於發現了腎上腺皮質激素並闡明其結構和生物學效應。兩位科學家的偉大發現使糖皮質激素這一具有重要生理功能的藥物得以套用於臨床,給醫學界帶來了很大的啟發和鼓舞,Edward與Philip也因此獲得了1950年
諾貝爾醫學獎。糖皮質激素如今已是臨床中最常用的免疫抑制劑,它可通過抑制巨噬細胞的吞噬功能,溶解淋巴細胞,減少針對自身抗原的自身抗體生成而抑制人體的免疫反應,廣泛套用於嚴重急性感染、過敏性疾病、組織器官移植的排斥反應及治療某些自身免疫性疾病等。
藥物新發現
伴隨醫學的不斷發展,免疫抑制劑家族的成員進一步擴大,人類征服疾病的能力也在不斷增強。1972年,氨甲喋呤(methotrexate,MTX)得到套用,它為抗葉酸類抗代謝藥物,對細胞免疫及體液免疫均具有免疫抑制作用。1978年,環孢黴素A(cyclos2poirinA,CsA)作為免疫製劑首次應於臨床,它為細胞因子合成抑制劑,抑制T細胞的細胞因子基因轉錄,阻斷T細胞產生,干擾T細胞活化。它在G0/G1期(G0、G1、S是細胸分裂周期中的不同階段)交界處阻斷T細胞激活,屬於T細胞早期激活的抑制劑。自20世紀80年代起,CsA被陸續推廣套用到各種器官和組織的移植,獲得了廣泛成功,開闢了器官移植的新時代。直至今日,CsA仍位居各種臨床移植抑制用藥之首。
FK506
FK506是繼CsA之後開發的另一種親免疫結合劑,它可預防多種移植排斥,尤適用於肝臟移植。FK506的免疫抑制作用約為CsA的10~100倍,其急、慢性排斥反應率低,感染率低,激素用量較少,可逆轉急性排斥反應,不良反應較CsA少,故有望取代CsA成為器官移植術後首選的免疫抑制劑。1989年,雷帕黴素(Rapamycin,RPM)首次被用於抗移植排斥,它可有效地預防排斥反應,與其它藥物合用,使急性排斥率下降。它可特異性干擾鈣離子依賴性通道,通過抑制P70S6蛋白激酶的磷酸化及其活性來抑制
細胞因子誘導的蛋白質及DNA合成。它在G1/S期交界處通過干擾非鈣依賴性途徑,阻斷細胞周期,為T細胞晚期激活抑制劑。通過相似的途徑,B細胞激活也可被直接影響,雷帕黴素作為一種新型免疫抑制劑,其作用不僅是抑制免疫細胞,而且抑制血管平滑肌增生和移行,減輕排斥反應。1995年,霉酚酸酯(mycophe鄄no2latemofetil,MMF)被美國FDA批准,並迅速套用於臨床,它療效高,對增殖的淋巴細胞有很高的選擇性作用,同時還能通過直接抑制B細胞增殖,阻止抗體的形成。此後一系列新型免疫抑制劑層出不窮,如生物免疫抑制劑抗淋巴細胞球蛋白(antilymphocyticglob2ulin,ALG)以及抗T細胞球蛋白(antiTcellglobulin,ATG)是藉助於多克隆抗體消除或抑制T細胞,已廣泛用於
腎、
肝、
心、
胰腺和
骨髓移植。20世紀80年代以來,研究者們研製出了一系列針對T細胞表面標誌、粘附分子、共刺激分子、抗原受體和細胞因子及其受體的單克隆抗體,有些已經在臨床套用或進入臨床評估階段。所有這些免疫抑制劑的開發,凝結了無數科學研究者們的心血和汗水,正是他們的辛苦勞動,使得免疫抑制劑的發展日臻完善。
 普通外科學
普通外科學副作用
免疫抑制劑由於選擇性和特異性的限制,在治療的同時不可避免地會損傷患者的免疫防衛能力,致使患者抗感染能力下降,惡性病變的危險增加,損傷造血、免疫系統及肝、腎、消化道功能,造成神經和內分泌功能紊亂,並引發某些過敏反應等。環磷醯胺可引起患者脫髮,致出血性膀胱炎,如尿頻、尿痛、血尿,蛋白尿等。糖皮質激素可加重或誘發感染,誘發胃潰瘍,合併出血和穿孔,引起代謝紊亂,升高
血壓、
血糖、
血脂,引起骨質疏鬆,興奮中樞神經系統致失眠等不良反應。硫唑嘌呤可致膽汁淤積和肝細胞損害。MTX有消化道損害症狀,如口腔潰瘍、血便等,尚可致畸胎、死胎。環孢黴素具有腎、肝及神經系統毒性,並可導致高血壓,繼發感染和腫瘤的發生。FK506也具有腎毒性,而且在神經毒性方面還甚於CsA,並對胰島β2細胞有損傷,誘發糖尿病。雷帕黴素可引起白細胞減少,血小板減少和高脂血症。霉酚酸脂則可引起嘔吐、腹瀉等胃腸道症狀、白細胞減少症、敗血症以及高血尿酸、高血鉀、肌痛或嗜睡等。一系列的不良反應使得一些病人在接受治療的同時,也飽嘗了免疫抑制劑大量長期套用而帶來的痛苦,有些病人病情變得更加複雜以至惡化,連
醫生也束手無策。
 普通外科學
普通外科學 普通外科學
普通外科學 普通外科學
普通外科學 普通外科學
普通外科學 普通外科學
普通外科學
 普通外科學
普通外科學 普通外科學
普通外科學 普通外科學
普通外科學 普通外科學
普通外科學